Инфаркт миокарда по отведениям. Как проявляется инфаркт миокарда на экг
28.04.2017
Инфаркт миокарда — одно из тяжелых заболеваний. Прогноз на прямую зависит от того, насколько правильно была проведена диагностика, и назначена адекватная терапия.
Чем раньше специалисты диагностируют заболевание, тем эффективнее будет лечение. Электрокардиография (ЭКГ) точнее всех исследований, именно она на 100% может подтвердить диагноз, либо же исключить его.
Сердечная кардиограмма
Человеческие органы пропускают слабый ток. Именно это, и позволяет с помощью прибора, который регистрирует электрические импульсы, поставить точный диагноз. Электрокардиограф состоит из:
- приспособления, усиливающего слабый ток;
- приспособления, измеряющего напряжение;
- записывающего устройства на автоматической основе.
По данным кардиограммы, которая выводится на экран или печатается на бумаге, специалист и ставит диагноз.
В сердце человека есть особые ткани, по другому их называют проводящей системой, они передают мышцам сигналы, указывающие на расслабление или сокращение органа.
Электрический ток в сердечных клетках поступает периодами, это:
- деполяризация. Отрицательный клеточный заряд сердечных мышц заменяется положительным;
- реполяризация. Восстанавливается отрицательный внутриклеточный заряд.
Поврежденная клетка имеет низкую электропроводность, чем здоровая. Именно это и фиксирует электрокардиограф.
Прохождение кардиограммы позволяет записать действие токов, которые возникают в работе сердца.
Когда ток отсутствует, то гальванометр фиксирует ровную линию (изолиния), а если клетки миокарда возбуждаются в разных фазах, то гальванометр фиксирует характерный зубец, направленный вверх или вниз.
Электрокардиографическая проверка фиксирует три стандартных отведения, усиленных три и грудных шесть. Если есть показания, то еще добавляют отведения, чтобы проверить задние сердечных отделы.
Каждое отведение электрокардиограф фиксирует отдельной линией, что в дальнейшем помогает диагностировать сердечные поражения.
В итоге комплексная кардиограмма имеет 12 графических линий, и каждая из них изучается.
На электрокардиограмме выделяются пять зубцов — P, Q,R,S,T, бывают случаи, когда добавляют еще и U. У каждого своя ширина, высота и глубина, а также направлен каждый в своем направлении.
Между зубцами есть интервалы, они тоже измеряются и изучаются. Также фиксируют интервальные отклонения.
Каждый зубец отвечает за функции и возможности определенных мышечных отделов сердца. Специалисты учитывают соотношение между ними (все зависит от высоты, глубины и направления).
Все эти показатели помогают отличить нормальную работу миокарда от нарушенной, вызванной разными патологиями.
Главная особенность электрокардиограммы заключается в выявлении и регистрации важных для диагностики и дальнейшего лечения симптомов патологии.
Определение инфаркта на экг
Из-за того, что начинают отмирать участки мышц сердца, начинает местно снижаться электрические возможности сравнительно с оставшимися неповрежденными тканями.
Именно, это и указывает где конкретно локализуется инфаркт миокарда. Малейшие изменения на экг указывают пораженные участки миокарда, которые возникают при ишемических сердечных болезнях:
- омертвение клеток — как правило, это происходит в центре органа, изменяется комплекс Q, R, S. В основном, образуется болезненный зубец Q;
- поврежденная зона — локализуется вокруг омертвевших клеток, на экг заметно, что смещен сегмент S,T;
- зона со сниженным кровообращением — находится на черте с не пораженным миокардом. Изменяется амплитуда и полярность зубца Т.
Изменения на электрокардиограмме определяет глубину омертвления клеток сердечных мышц:
- трансмуральный инфаркт миокарда — на графическом изображении выпадает зубец R, и вместо комплекса Q,R,S получается Q.S;
- субэпикардиальный инфаркт миокарда — указывает на сегментарную депрессию S, T. причем изменяется сам зубец Т, при этом комплекс Q, R, S — не меняется;
- интрамуральный инфаркт миокарда сопровожден изменениями Q, R, S и высотой сегмента S, T, который сопровождается слиянием с положительным зубцом Т.
Признаки инфаркта миокарда на экг имеет три этапа развития:
- первый этап может длиться от пару часов до 68 (трое суток). При проведении электрокардиограммы специалисты замечают, что сегмент ST поднимается (получается подъем в виде купола) и сливается с положительным зубцом. Сегмент начинается низко сходящего зубца. В этом случае на изображении появляется зубец Q, он считается патологическим.
- второй этап, подострый. Может длиться около месяца, иногда и двух. На кардиограмме фиксируется сниженный сегмент S, T и он приближается к изолинии. Формируется отрицательный зубец Т и увеличивается патологический Q.
- третий этап — рубцовый. Может длиться очень долго. Миокард имеет вид постинфарктного кардиосклероза и его могут фиксировать на электрокардиограмме на протяжении всей жизни у пациента, который перенес инфаркт. Рубцовый этап изображается на экг в виде сниженного сегмента S, T. Он снижается до уровня изолинии и формирует негативный характерный зубец Т, который имеет треугольный вид. Зубец Q остается неизменным. Через некоторое время он не исчезает, а просто сглаживается, и постоянно определяется врачами.
 У большинства пациентов сердечная динамика на электрокардиограмме не совпадает с морфологическим изменение мышц сердца.
У большинства пациентов сердечная динамика на электрокардиограмме не совпадает с морфологическим изменение мышц сердца.
Например, при проведении экг, врачи определили рубцовый этап развития инфаркта, но при этом рубцовая ткань еще не начала формироваться.
Или наоборот, второй этап (подострый) определяется на электрокардиограмме несколько месяцев, при этом рубец уже окончательно сформированный.
Поэтому при постановке диагноза, врачи учитывают не только расшифровку кардиограммы и стадии инфаркта, но и клинические проявления патологии и результаты лабораторных исследований.
Как определить где локализуется инфаркт на экг
Практически во всех случаях при уменьшенном кровоснабжении инфаркт локализуется в левом желудочке мышечного слоя сердца, справа — диагностируется в редких случаях. Поражается передняя, боковая и задняя часть.
При проведении ЭКГ признаки инфаркта миокарда определяются в отведениях:
- Ишемическая болезнь сердца в передней части указывает на нарушения в отведениях груди — V1, V2, V3, 1 и 2 — это нормальный показатель, а в усиленном случае AVL.
- Ишемия на боковых стенках отдельно диагностируется редко, чаще локализуется на передних и задних стенках левого желудочка, нарушения заметны в отведениях V3, V4, V5 в дополнении с 1 и 2 нормальными показателями, а в усиленном случае AVL.
- Ишемия на задней стенке имеет два вида: диафрагмальный (патологические нарушения определены отведении усиленного характера AVF, также затрагивается второе и третье отведение; базальный — увеличивается зубец R в левом отведении грудины.
Ишемическая болезнь сердца в области правого желудочка и предсердия диагностируются в редких случаях, в основном, прикрываются признаками сердечных поражений в левом отделе.
Может ли кардиограмма определить обширность инфаркта
На распространенность сердечных поражений указывают изменения в отведениях. По этим данным различают два вида инфаркта миокарда:
- Мелкоочаговый указывает на отрицательные показатели Т, при этом смещен сегментальный интервал S, T, а патологические резцы R, Q не наблюдаются.
- Распространенный вызван всеми измененными отведениями.
Определение глубины омертвения мышечного слоя
Инфаркт различается по глубине омертвения сердечных стенок:
- субэпикардиальный — поражается зона под наружным сердечным слоем;
- субэндокардиальный — омертвение происходит возле внутреннего слоя;
- трансмуральный — поражается вся толща миокарда.
Проведенная кардиограмма при инфаркте всегда определяет глубину некроза.
Сложности при электрокардиографии

Современная медицина и новые аппараты ЭКГ в состоянии легко проводить расчеты (это происходит автоматически). С помощью холтеровского мониторирования можно фиксировать работу сердца на протяжении суток.
В современных палатах стоит кардиомониторное наблюдение и имеет звуковой сигнал тревоги, это позволяет врачами замечать измененные сердечные сокращения.
Окончательный диагноз ставится специалистом по результатам электрокардиограммы, клинических проявлений.
На ЭКГ при инфаркте миокарда (фото 1) врачи четко видят признаки некроза сердечной ткани. Кардиограмма при инфаркте является достоверным диагностическим методом и позволяет определить степень поражения сердца.

Расшифровка ЭКГ при инфаркте миокарда
Электрокардиограмма является безопасным методом исследования, а при подозрении на случившийся инфаркт – просто незаменимым. ЭКГ при инфаркте миокарда основывается на нарушении сердечной проводимости, т.е. в определенных участках кардиограммы врач увидит аномальные изменения, которые свидетельствуют об инфаркте. Для получения достоверной информации врачи используют 12 электродов при снятии данных. Кардиограмма при инфаркте миокарда (фото 1) регистрирует такие изменения на основании двух фактов:
- при инфаркте у человека нарушается процесс возбуждения кардиомиоцитов, причем происходит это после омертвения клеток;
- в тканях сердца, пораженных инфарктом, нарушается электролитный баланс – калий в значительной степени покидает поврежденные патологий ткани.
Эти изменения дают возможно регистрировать на электрокардиографе линии, являющиеся признаками нарушения проводимости. Развиваются они не сразу, а только лишь через 2-4 часа в зависимости от компенсаторных возможностей организма. Тем не менее, кардиограмма сердца при инфаркте показывает сопутствующие ему признаки, по которым можно определить нарушение работы сердца. Фото с расшифровкой кардиологическая бригада скорой помощи высылает в ту клинику, где будут принимать такого больного – врачи-кардиологи будут заранее готовы к тяжелому пациенту.
Выглядит инфаркт миокарда на ЭКГ (фото внизу) следующим образом:
- полное отсутствие зубца R или его значительное уменьшение по высоте;
- крайне глубокий, проваливающийся зубец Q;
- приподнятый S-T сегмент над уровнем изолинии;
- наличие отрицательного зубца T.
Электрокардиограмма показывает и различные стадии инфаркта. Инфаркт на ЭКГ (фото в гал.) может быть подострым, когда изменения в работе кардиомиоцитов только начинают появляться, острым, острейшим и на стадии рубцевания.
Также электрокардиограмма позволяет оценить врачу следующие параметры:
- диагностировать сам факт случившегося инфаркта;
- определить область, где произошли патологические изменения;
- установить давность возникших изменений;
- определиться с тактикой лечения больного;
- прогнозировать возможность летального исхода.
Трансмуральный инфаркт миокарда – один из самых опасных и тяжелых видов повреждения сердца. Его еще называют крупноочаговым или Q-инфарктом. Кардиограмма после инфаркта миокарда (фото ниже) с крупноочаговым поражением показывает, что зона отмирания клеток сердца захватывает всю толщины сердечной мышцы.

Инфаркт миокарда
Инфаркт миокарда является следствием ишемической болезни сердца. Чаще всего к ишемии приводит атеросклероз сердечных сосудов, спазм или закупорка. Случиться инфаркт (фото 2) может и в результате хирургического вмешательства, если проводится перевязка артерии или выполняется ангиопластика.
Ишемический инфаркт проходит четыре стадии течения патологического процесса:
- ишемия, при которой клетки сердца перестают получать необходимый объем кислорода. Эта стадия может длиться довольно долго, поскольку организм включает все компенсаторные механизмы для обеспечения нормальной работы сердца. Непосредственным механизмом возникновения ишемии является сужение сердечных сосудов. До какого-то момента сердечная мышца с таким недостатком кровообращения справляется, но, когда тромбоз сужает сосуд до критических размеров, сердце больше не в состоянии компенсировать недостачу. Обычно для этого необходимо сужение артерии на 70 процентов и более;
- повреждения, происходящие непосредственно в кардиомиоцитах, которые начинаются уже через 15 минут после прекращения кровообращения в поврежденной зоне. Инфаркт сердца длится примерно 4-7 часов. Именно здесь у пациента начинаются характерные признаки инфаркта – боли за грудиной, тяжесть, аритмия. Обширный инфаркт сердца (фото внизу) – наиболее тяжелый исход приступа, при таком повреждении зона омертвения может доходить до 8 см в ширину;
- некроз – омертвение клеток сердца и прекращение выполнения ими своих функций. В данном случае происходит отмирание кардиомиоцитов, некроз не дает им возможности выполнять свои функции;
- рубцевание – замещение омертвевших клеток соединительнотканными образованиями, не способными брать на себя функцию предшественников. Такой процесс начинается практически сразу же после омертвения и понемногу на 1-2 недели на сердце в месте повреждения формируется соединительнотканный рубец из фибриновых волокон.
Геморрагический инфаркт головного мозга является родственным состоянием по механизмам повреждения, однако он представляет собой выход крови из сосудов головного мозга, которые препятствуют работе клеток.

Сердце после инфаркта
Сердце после инфаркта миокарда (фото 3) подвергается процессу кардиосклероза. Соединительная ткань, которая замещает кардиомиоциты, превращается в грубый рубец – его могут увидеть патологоанатомы при вскрытии людей, перенесших инфаркт миокарда.
Рубец после инфаркта миокарда имеет различную толщину, длину и ширину. Все эти параметры влияют на дальнейшую деятельность сердца. Глубокие и большие по площади очаги склерозирования носят название обширного инфаркта. Восстановление после такой патологии крайне сложное. При микросклерозировании инфаркт, как и , может оставлять минимальные повреждения. Зачастую пациенты даже не знают, что перенесли такое заболевание, поскольку признаки были минимальными.
Рубец на сердце после инфаркта (фото в гал.) в дальнейшем не болит и не дает о себе знать примерно 5-10 лет после инфаркта, однако он провоцирует перераспределение сердечной нагрузки на здоровые области, которые теперь должны выполнять больше работы. Через определенное время выглядит сердце после инфаркта (фото ниже) изношенным – орган не может выполнять нагрузку, ишемическая болезнь сердца у пациентов усугубляется, появляются боли в сердце, одышка, они быстро утомляются, требуется постоянная медикаментозная поддержка.
Галерея фото инфаркта миокарда
(ИМ) остается самой частой причиной вызовов бригад скорой медицинской помощи (СМП). Динамика количества вызовов в г. Москве по поводу ИМ на протяжении трех лет (табл. 1.) отражает стабильность количества вызовов «скорой помощи» по поводу ИМ на протяжении трех лет и постоянство соотношения осложненных и неосложненных инфарктов миокарда. Что касается госпитализаций, то общее их количество практически не изменилось с 1997 до 1999 г. В то же время снизился процент госпитализаций больных с неосложненным ИМ на 6,6% с 1997 к 1999 г.
Таблица 1. Структура вызовов к больным ИМ.
|
Показатель |
1997 |
1998 |
1999 |
|
Количество вызовов к больным ИМ |
|||
|
Неосложненным |
16255 |
16156 |
16172 |
|
Осложненным |
7375 |
7383 |
7318 |
|
Всего |
23630 |
23539 |
23490 |
|
% к общему числу больных сердечно-сосудистыми заболеваниями |
|||
|
Госпитализировано больных |
|||
|
Неосложненным ИМ |
11853 |
12728 |
11855 |
|
Осложненным ИМ |
3516 |
1593 |
3623 |
|
Всего |
15369 |
16321 |
15478 |
|
% госпитализированных больных к количеству вызовов |
|||
|
Неосложненнным ИМ |
79,9 |
78,8 |
73,3 |
|
Осложненным ИМ |
47,6 |
48,7 |
49,5 |
|
Всего |
65,0 |
69,3 |
65,9 |
ОПРЕДЕЛЕНИЕ
Инфаркт миокарда - неотложное клиническое состояние, обусловленное некрозом участка сердечной мышцы в результате нарушения ее кровоснабжения.
ОСНОВНЫЕ ПРИЧИНЫ ВОЗНИКНОВЕНИЯ И ПАТОГЕНЕЗ
Развивающийся в рамках ишемической болезни сердца, является результатом коронарного . Непосредственной причиной инфаркта миокарда чаще всего служит окклюзия или субтотальный стеноз коронарной артерии, почти всегда развивающийся вследствие разрыва или расщепления атеросклеротической бляшки с образованием тромба, повышенной агрегацией тромбоцитов и сегментарным спазмом вблизи бляшки.
КЛАССИФИКАЦИЯ
С точки зрения определения объема необходимой лекарственной терапии и оценки прогноза представляют интерес три классификации.
А. По глубине поражения (на основе данных электрокардиографического исследования):
1. Трансмуральный и крупноочаговый («Q-инфаркт») - с подъемом сегмента ST в
Первые часы заболевания и формированием зубца Q в последующем.
2. Мелкоочаговый («не Q-инфаркт») - не сопровождающийся формированием зубца Q, а
Проявляющийся отрицательными зубцами Т
Б. По клиническому течению:
1. Неосложненный инфаркт миокарда.
2. Осложненный инфаркт миокарда (см. ниже).
В. По локализации:
1. Инфаркт левого желудочка (передний, задний или нижний, перегородочный)
2. Инфаркт правого желудочка.
КЛИНИЧЕСКАЯ КАРТИНА
По симптоматике острейшей фазы инфаркта миокарда выделяют следующие клинические варианты:
|
Болевой (status anginosus) |
- типичное клиническое течение, основным проявлением при котором служит ангинозная боль, не зависящая от позы и положения тела, от движений и дыхания, устойчивая к нитратам; боль имеет давящий, душащий, жгущий или раздирающий характер с локализацией за грудиной, во всей передней грудной стенке с возможной иррадиацией в плечи, шею, руки, спину, эпигастальную область; характерны сочетание с гипергидрозом, резкой общей слабостью, бледностью кожных покровов, возбуждением, двигательным беспокойством. |
|
Абдоминальный (status gastralgicus) |
- проявляется сочетанием эпигастральных болей с диспептическими явлениями - тошнотой, не приносящей облегчения рвотой, икотой, отрыжкой, резким вздутием живота; возможны ирадиация болей в спину, напряжение брюшной стенки и болезненность при пальпации в эпигастрии. |
|
Атипичный болевой |
- при котором болевой синдром имеет атипичный характер по локализации (например, только в зонах иррадиации - горле и нижней челюсти, плечах, руках и т.д.) и/или по характеру. |
|
Астматический (status astmaticus) |
- единственным признаком при котором является приступ одышки, являющийся проявлением острой застойной сердечной недостаточности (сердечная астма или отек легких). |
|
Аритмический |
- при котором нарушения ритма служат единственным клиническим проявлением или преобладают в клинической картине. |
|
Цереброваскулярный |
- в клинической картине которого преобладают признаки нарушения мозгового кровообращения (чаще - динамического): обморок, головокружение, тошнота, рвота; возможна очаговая неврологическая симптоматика. |
|
Малосимптомный (бессимптомный) |
- наиболее сложный для распознавания вариант, нередко диагностируемый ретроспективно по данным ЭКГ. |
ДИАГНОСТИЧЕСКИЕ КРИТЕРИИ
На догоспитальном этапе оказания медицинской помощи диагноз острого инфаркта миокарда ставится на основании наличия соответствующих:
а) клинической картины
б) изменений электрокардиограммы.
А. Клинические критерии.
При болевом варианте инфаркта диагностическим значением обладают:
- интенсивность (в случаях, когда аналогичные боли возникали ранее, при инфаркте они бывают необычно интенсивными),
- продолжительность (необычно длительный приступ, сохраняющийся более 15-20 минут),
- поведение больного (возбуждение, двигательное беспокойство),
- неэффективность сублингвального приема нитратов.
Таблица 2.
Перечень вопросов, обязательных при анализе болевого синдрома в случае подозрения на острый инфаркт миокарда
|
Вопрос |
Примечание |
|
Когда начался приступ? |
Желательно определить как можно точнее. |
|
Сколько времени длится приступ? |
Менее 15, 15-20 или более 20 мин. |
|
Были ли попытки купировать приступ нитроглицерином? |
Был ли хотя бы кратковременный эффект? |
|
Зависит ли боль от позы, положения тела, движений и дыхания? |
При коронарогенном приступе не зависит. |
|
Были ли аналогичные приступы в прошлом? |
Аналогичные приступы, не завершившиеся инфарктом, требуют дифференциальной диагностики с нестабильной стенокардией и не кардиальными причинами. |
|
Возникали ли приступы (боли или удушья) при физической нагрузке (ходьбе), заставляли ли они останавливаться, сколько они длились (в минутах), как реагировали на нитроглицерин? |
Наличие стенокардии напряжения делает весьма вероятным предположение об остром инфаркте миокарда. |
|
Напоминает ли настоящий приступ ощущения, возникавшие при физической нагрузке по локализации или характеру болей? |
По интенсивности и сопровождающим симптомам приступ при инфаркте миокарда обычно более тяжелый, чем при стенокардии напряжения. |
При любом варианте вспомогательное диагностическое значение имеют:
Гипергидроз,
Резкая общая слабость,
Бледность кожных покровов,
Признаки острой сердечной недостаточности.
Отсутствие типичной клинической картины не может служить доказательством отсутствия инфаркта миокарда.
Б. Электрокардиографические критерии - изменения, служащие признаками:
|
Повреждения |
- дугообразный подъем сегмента ST выпуклостью вверх, сливающийся с положительным зубец T или переходящий в отрицательный зубец T (возможна дугообразная депрессия сегмента ST выпуклостью вниз); |
|
Крупноочагового или Трансмурального инфаркта |
- появление патологического зубца Q и уменьшение амплитуды зубца R или исчезновение зубца R и формирование QS; |
|
Мелкоочагового инфаркта |
- появление отрицательного симметричного зубца T; |
|
Примечания: 1. Косвенным признаком инфаркта миокарда, не позволяющим определить фазу и глубину процесса, является остро возникшая блокада ножек пучка Гиса (при наличии соответствующей клиники). 2. Наибольшей достоверностью обладают электрокардиографические данные в динамике, поэтому электрокардиограммы при любой возможности должны сравниваться с предыдущими. |
|
При инфаркте передней стенки подобные изменения выявляются в I и II стандартных отведениях, усиленном отведении от левой руки (aVL) и соответствующих грудных отведениях (V1, 2, 3, 4, 5, 6). При высоком боковом инфаркте миокарда изменения могут регистрироваться только в отведении aVL и для подтверждения диагноза необходимо снять высокие грудные отведения. При инфаркте задней стенки (нижнем, диафрагмальном) эти изменения обнаруживаются во II, III стандартном и усиленном отведении от правой ноги (aVF). При инфаркте миокарда высоких отделов задней стенки левого желудочка (задне-базальном) изменения в стандартных отведениях не регистрируется, диагноз ставится на основании реципрокных изменений - высоких зубцов R и Т в отведениях V 1 -V 2 (таблица 3).
Рис. 1. Острейшая фаза трансмурального переднего инфаркта миокарда.
Таблица 3. Локализация инфаркта миокарда по данным ЭКГ
|
Тип инфаркта по локализации |
Стандартные отведения |
Грудные отведения |
|||||||||
|
III |
|||||||||||
|
Перегородочный |
|||||||||||
|
Пердне-перегородочный |
|||||||||||
|
Передний |
|||||||||||
|
Распростаненный передний |
|||||||||||
|
Передне-боковой |
|||||||||||
|
Боковой |
|||||||||||
|
Высокий боковой |
|||||||||||
|
Задне-боковой |
|||||||||||
|
Задне-диафрагмальный |
|||||||||||
|
Задне-базальный |
|||||||||||
ЛЕЧЕНИЕ ИНФАРКТА МИОКАРДА
Неотложная терапия преследует несколько взаимосвязанных целей:
1. Купирование болевого синдрома.
2. Восстановление коронарного кровотока.
3. Уменьшение работы сердца и потребности миокарда в кислороде.
4. Ограничение размеров инфаркта миокарда.
5. Лечение и профилактика осложнений инфаркта миокарда.
Применяемые для этого лекарственные средства представлены в таблице 3.
Таблица 3.
Основные направления терапии и лекарственные средства, применяемые в острейшей стадии неосложненного инфаркта миокарда
|
Лекарственное средство |
Направления терапии |
|
|
Морфин внутривенно дробно |
Адекватное обезболивание, снижение пред- и постнагрузки, психо-моторного возбуждения, потребности миокарда в кислороде |
2-5 мг внутривенно каждые 5-15 минут до полного устранения болевого синдрома либо до появления побочных эффектов |
|
Стрептокиназа (стрептаза) |
Восстановление коронарного кровотока (тромболизис), купирование болевого синдрома, ограничение размеров инфаркта миокарда, снижение летальности |
1,5 млн. МЕ внутривенно за 60 минут |
|
Гепарин внутривенно струйно (если не проводится тромболизис) |
Предупреждение или ограничение коронарного тромбоза, профилактика тромбоэмболических осложнений, снижение летальности |
10000-15000 МЕ внутривенно струйно |
|
Нитроглицерин или изосорбида динитрат внутривенно капельно |
Купирование болевого синдрома, уменьшение размеров инфаркта миокарда и летальности |
10 мкг/мин. с увеличением скорости на 20 мкг/мин каждые 5 минут под контролем ЧСС и АД |
|
Бета-адреноблокаторы: пропранолол (обзидан) |
Снижение потребности миокарда в кислороде, купирование болевого синдрома, уменьшение размеров некроза, профилактика фибрилляции желудочков и разрыва левого желудочка, повторных инфарктов миокарда, снижение летальности |
1 мг/мин каждые 3-5 минут до общей дозы 10 мг |
|
Ацетилсалици-ловая кислота (аспирин) |
Купирование и профилактика процессов, связанных с агрегацией тромбоцитов; при раннем(!) назначении снижает летальность |
160-325 мг разжевать; |
|
Магния сульфат (кормагнезин) |
Снижение потребности миокарда в кислороде, купирование болевого синдрома, уменьшение размеров некроза, профилактика нарушений сердечного ритма, сердечной недостаточности, снижение летальности |
1000 мг магния (50 мл 10 %, 25 мл 20 % или 20 мл 25 % раствора) внутривенно в течение 30 минут. |
АЛГОРИТМ ОКАЗАНИЯ МЕДИЦИНСКОЙ ПОМОЩИ БОЛЬНЫМ ОСТРЫМ ИНФАРКТОМ МИОКАРДА НА ДОГОСПИТАЛЬНОМ ЭТАПЕ
А. Неосложненный инфаркт миокарда

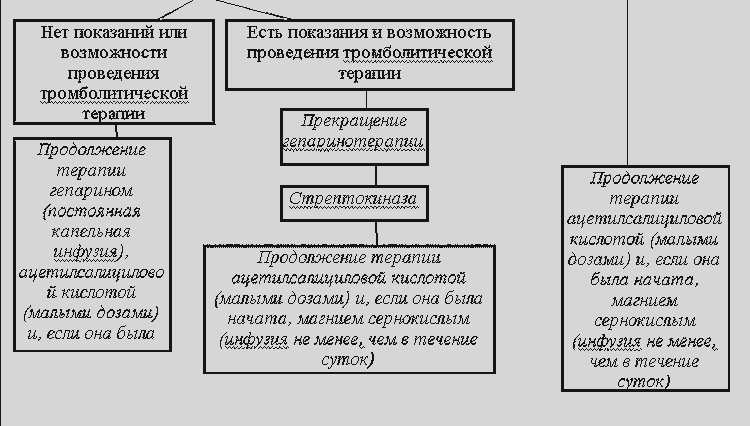
Б. Неосложненный инфаркт миокарда или инфаркт миокарда, осложненный упорным болевым синдромом

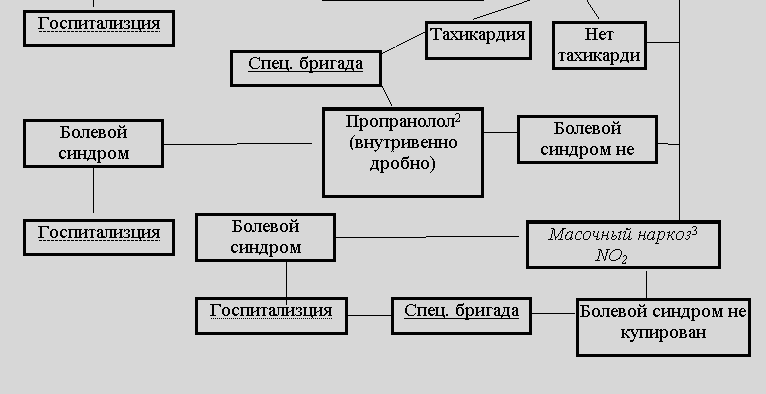
В. Осложненный инфаркт миокарда

1. Купирование болевого приступа
при остром инфаркте миокарда - одна из важнейших задач, поскольку боль через активацию симпатоадреналовой системы вызывает повышение сосудистого сопротивления, частоты и силы сердечных сокращений, то есть увеличивает гемодинамическую нагрузку на сердце, повышает потребность миокарда в кислороде и усугубляет ишемию.
Если предварительный сублингвальный прием нитроглицерина (повторно по 0,5 мг в таблетках или 0,4 мг в аэрозоле) боль не купировал, начинается терапия наркотическими анальгетиками, обладающими кроме анальгетического и седативного действия влиянием на гемодинамику: вследствие вазодилатирующих свойств они обеспечивают гемодинамическую разгрузку миокарда, уменьшая в первую очередь преднагрузку. На догоспитальном этапе препаратом выбора для купирования болевого синдрома при инфаркте миокарда является морфин, обладающий не только необходимыми эффектами, но и достаточной для транспортировки длительностью действия. Препарат вводится внутривенно дробно: 1 мл 1 % раствора разводят физиологическим раствором натрия хлорида до 20 мл (1 мл полученного раствора содержит 0,5 мг активного вещества) и вводят 2-5 мг каждые 5-15 минут до полного устранения болевого синдрома либо до появления побочных эффектов (гипотензии, угнетения дыхания, рвоты). Суммарная доза не должна превышать 10-15 мг (1-1,5 мл 1% раствора) морфина (на догоспитальном этапе не допускается превышение дозы 20 мг).
При невыраженном болевом синдроме, пациентам старческого возраста и ослабленным больным наркотические анальгетики могут вводиться подкожно или внутримышечно. Не рекомендуется вводить подкожно более 60 мг морфина в течение 12 часов.
Для профилактики и купирования таких побочных эффектов наркотических анальгетиков как тошнота и рвота рекомендуют внутривенное введение 10-20 мг метоклопрамида ( , реглана). При выраженной брадикардии с гипотонией или без нее показано использование атропина в дозе 0,5 мг (0,5 мл 0,1 % раствора) внутривенно; борьба же со снижением артериального давления проводится по общим принципам коррекции гипотензии при инфаркте миокарда.
Недостаточная эффективность обезболивания наркотическими анальгетиками служит показанием к внутривенной инфузии нитратов. При низкой эффективности нитратов в сочетании с тахикардией дополнительный обезболивающий эффект может быть получен введением бета-адреноблокаторов. Боль может быть купирована в результате эффективного тромболизиса.
Упорные интенсивные ангинозные боли служат показанием к применению масочного наркоза закисью азота (обладающей седативным и анальгезирующим действием) в смеси с кислородом. Начинают с ингаляции кислорода в течение 1-3 минут, затем используется закись азота (20 %) с кислородом (80 %) с постепенным повышением концентрации закиси азота до 80 %; после засыпания больного переходят на поддерживающую концентрацию газов - 50 ´ 50 %. Положительный момент - закись азота не влияет на функцию левого желудочка. Возникновение побочных эффектов - тошноты, рвоты, возбуждения или спутанности сознания - является показанием для уменьшения концентрации закиси азота или отмены ингаляции. При выходе из наркоза ингалируют чистый кислород в течение 10 минут для предупреждения артериальной гипоксемии.
Для решения вопроса о возможности использования наркотических анальгетиков следует уточнить ряд моментов:
- убедиться, что типичный или атипичный болевой синдром не является проявлением “острого живота”, и изменения ЭКГ являются специфическим проявлением инфаркта миокарда, а не неспецифической реакцией на катастрофу в брюшной полости;
- выяснить, имеются ли в анамнезе хронические заболевания системы дыхания, в частности, бронхиальная астма;
- уточнить, когда было последнее обострение бронхообструктивного синдрома;
- установить, имеются ли в настоящее время признаки дыхательной недостаточности, какие, какова степень ее выраженности;
- выяснить, имеется ли у больного в анамнезе судорожный синдром, когда был последний припадок.
2. Восстановление коронарного кровотока в острейшей фазе инфаркта миокарда,
достоверно улучшающее прогноз, при отсутствии противопоказаний осуществляется путем системного тромболизиса.
А). Показаниями к проведению тромболизиса служат наличие подъема сегмента ST более чем на 1 mm по крайней мере в двух стандартных отведениях ЭКГ и более чем на 2 mm в двух смежных грудных отведениях или остро возникшая полная блокада левой ножки пучка Гиса при сроке, прошедшем с начала заболевания, более 30 минут, но не превышающем 12 часов. Применение тромболитических средств возможно и позже в случаях когда сохраняются подъем сегмента ST, продолжается боль и/или наблюдается нестабильная гемодинамика.
В отличие от внутрикоронарного системный тромболизис (осуществляется внутривенным введением тромболитических средств) не требует каких-либо сложных манипуляций и специального оборудования. При этом он достаточно эффективен, если начат в первые часы развития инфаркта миокарда (оптимально - на догоспитальном этапе), поскольку сокращение летальности на прямую зависит от сроков его начала.
При отсутствии противопоказаний решение вопроса о проведении тромболизиса основывается на анализе фактора времени: если транспортировка в соответствующий стационар может быть продолжительнее, чем срок до начала этой терапии специализированной бригадой “скорой помощи” (при предполагаемом времени транспортировки более 30 минут или при отсрочке внутрибольничного проведения тромболизиса более чем на 60 минут), введение тромболитических средств должно осуществляться на догоспитальном этапе оказания медицинской помощи. В противном случае оно должно быть отложено до госпитального этапа.
Наиболее часто используется стрептокиназа. Методика внутривенного введения стрептокиназы: введение стрептокиназы проводится только через периферические вены, попытки катетеризации центральных вен недопустимы; перед инфузией возможно внутривенное введение 5-6 мл 25% магния сульфата, либо 10 мл кормагнезина-200 в/в струйно, медленно (за 5 мин); «нагрузочная» доза аспирина (250-300 мг - разжевать) дается всегда, за исключением случаев, когда аспирин противопоказан (аллергические и ); 1 500 000 Ед стрептокиназы разводится в 100 мл изотонического раствора хлорида натрия и вводится внутривенно за 30 мин.
Одновременное назначение гепарина при использовании стрептокиназы не требуется - предполагают, что стрептокиназа сама обладает антикоагуляционными и антиагрегационными свойствами. Показано, что внутривенное введение гепарина не снижает летальность и частоту рецидивов инфаркта миокарда, а эффективность его подкожного введения сомнительна. Если гепарин по каким-либо причинам был введен ранее, это не является препятствием к проведению тромболизиса. Рекомендуется назначение гепарина через 4 ч после прекращения инфузии стрептокиназы. Рекомендовавшееся ранее использование гидрокортизона для профилактики анафилаксии признано не только малоэффективным, но и небезопасным в острейшей стадии инфаркта миокарда (глюкокортикоиды увеличивают риск разрыва миокарда).
Основные осложнения тромболизиса
1). Кровотечения (в т.ч. наиболее грозные - внутричерепные) - развиваются вследствие угнетения процессов свертывания крови и лизиса кровяных сгустков. Риск развития инсульта при системном тромболизисе составляет 0,5-1,5% случаев, обычно инсульт развивается в первые сутки после проведения тромболизиса. Для остановки незначительного кровотечения (из места пункции, изо рта, носа) достаточно сдавления кровоточащего участка. При более значимых кровотечениях (желудочно-кишечном, внутричерепном) необходима внутривенная инфузия аминокапроновой кислоты - 100 мл 5% раствора вводят в течение 30 мин и далее 1 г/час до остановки кровотечения, или транексамовой кислоты по 1-1,5 г 3-4 раза в сутки внутривенно капельно; кроме того эффективно переливание свежезамороженной плазмы. Следует однако помнить о том, что при использовании антифибринолитических средств возрастает риск реокклюзии коронарной артерии и реинфаркта, поэтому использовать их необходимо лишь при угрожающих жизни кровотечениях.
2). Аритмии, возникающие после восстановления коронарного кровообращения (реперфузионные). Не требуют интенсивной терапии медленный узловой или желудочковый ритм (при частоте сердечных сокращений менее 120 в мин и стабильной гемодинамике); наджелудочковая и желудочковая экстрасистолия (в том числе аллоритмированная); атриовентрикулярная блокада I и II (типа Мобитц I) степени. Требуют неотложной терапии фибрилляция желудочков (необходимы дефибрилляция, комплекс стандартных реанимационых мероприятий); двунаправленная веретенообразная желудочковая тахикардия типа «пируэт» (показаны дефибрилляция, введение сульфата магния внутривенно струйно); иные разновидности желудочковой тахикардии (используют введение лидокаина либо проводят кардиоверсию); стойкая суправентрикулярная тахикардия (купируется внутривенным струйным введением верапамила или новокаинамида); атриовентрикулярная блокада II (типа Мобитц II) и III степени, синоатриальная блокада (внутривенно струйно вводят атропин в дозе до 2,5 мг, при необходимости проводят экстренную электрокардиостимуляцию).
3). Аллергические реакции. Сыпь, зуд, периорбитальный отек встречаются в 4,4% случаев, тяжелые реакции ( , анафилактический шок) - в 1,7% случаев. При подозрении на развитие анафилактоидной реакции необходимо немедленно остановить инфузию стрептокиназы и ввести внутривенно болюсом 150 мг преднизолона. При выраженном угнетении гемодинамики и появлении признаков анафилактического шока внутривенно вводят 1 мл 1% раствора адреналина, продолжая введение стероидных гормонов внутривенно капельно. При лихорадке назначают аспирин или парацетамол.
4). Рецидивирование болевого синдрома после проведения тромболизиса купируется внутривенным дробным введением наркотических анальгетиков. При нарастании ишемических изменений на ЭКГ показано внутривенное капельное введение нитроглицерина или, если инфузия уже налажена, - увеличение скорости его введения.
5). При артериальной гипотонии в большинстве случаев бывает достаточно временно прекратить инфузию тромболитика и поднять ноги пациента; при необходимости уровень АД корректируется введением жидкости, вазопрессоров (допамина или норадреналина внутривенно капельно до стабилизации систолического АД на уровне 90-100 мм рт.ст.).

Рис. 2. Реперфузионная аритмия при трансмуральном заднем инфаркте миокарда: эпизод узлового ритма с самостоятельным восстановлением синусового ритма.
Клинические признаки восстановления коронарного кровотока:
- прекращение ангинозных приступов через 30-60 мин после введения тромболитика,
- стабилизация гемодинамики,
- исчезновение признаков левожелудочковой недостаточности,
- быстрая (в течение нескольких часов) динамику ЭКГ с приближением сегмента ST к изолинии и формированием патологического зубца Q, отрицательного зубца Т (возможно внезапное увеличение степени подъема сегмента ST с последующим его быстрым снижением),
- появление реперфузиооных аритмий (ускоренного идиовентрикулярного ритма, желудочковой экстрасистолии и др.),
- быстрая динамику МВ-КФК (резкое повышение ее активности на 20-40%).
Для решения вопроса о возможности использования тромболитичечских средств следует уточнить ряд моментов:
- убедиться в отсутствии в течение предшествовавших 10 дней острых внутренних кровотечений - желудочно-кишечного, легочного, маточного за исключением менструального , гематурии и др. (обратить внимание на их наличие в анамнезе) или хирургических вмешательств и травм с повреждением внутренних органов;
- исключить наличие в течение предшествовавших 2 месяцев острое нарушение мозгового кровообращения, операции или травмы головного или спинного мозга (обратить внимание на их наличие в анамнезе);
- исключить подозрение на острый панкреатит, расслаивающую аневризму аорты, а также на аневризму церебральной артерии, опухоль головного мозга или метастазирующие злокачественные опухоли;
- установить отсутствие физикальных признаков или анамнестических указаний на патологию свертывающей системы крови - геморрагический диатез, тромбоцитопения (обратить внимание на гаморрагическую диабетическую ретинопатию);
- убедиться, что больной не получает непрямые антикоагулянты;
- уточнить, не было ли аллергических реакций на соответствующие тромболитические препараты, а в отношении стрептокиназы, не было ли предшествовавшего ее введения в сроки от 5 дней до 2 лет (в этот период в связи с высоким титром антител введение стрептокиназы недопустимо);
- в случае проведенных успешных реанимационных мероприятий убедиться, что они не были травматичными и длительными (при отсутствии признаков постреанимационных травм - переломов ребер и повреждения внутренних органов обратить внимание на длительность, превышавшую 10 минут);
- добиться стабилизации повышенного артериального давления на уровне менее 200/120 мм рт. ст. (обратить внимание на уровень, превышающий 180/110 мм рт. ст.)
- обратить внимание на другие состояния , опасные развитием геморрагических осложнений и служащие относительными противопоказаниями к проведению системного тромболизиса: тяжелые заболевания печени или почек; подозрение на хроническую аневризму сердца, перикардит, инфекционный миокардит, наличие тромба в сердечных полостях; тромбофлебит и флеботромбоз; варикозное расширение вен пищевода, язвенная болезнь в стадии обострения; беременность;
- иметь в виду, что ряд факторов, не являющиеся относительными или абсолютными противопоказаниями к проведению системного тромболизиса, могут повышать его риск: возраст свыше 65 лет, масса тела менее 70 кг, женский пол, артериальная гипертензия.
Системный тромболизис возможен в пожилом и старческом возрасте, а также на фоне артериальной гипотензии (систолическое АД менее 100 мм рт. ст.) и кардиогенного шока.
В сомнительных случаях решение о проведении тромболитической терапии должно быть отсрочено до стационарного этапа лечения. Отсрочка показана при атипичном развитии заболевания, неспецифических изменениях ЭКГ, давно существующей блокаде ножки пучка Гиса и несомненном предшествующем инфаркте миокарда, маскирующем типичные изменения.
Б). Отсутствие показаний к тромболитической терапии (поздние сроки, так называемый мелкоочаговый или не-Q-инфаркт), невозможность проведения тромболизиса по организационным причинам, а также его отсрочка до госпитального этапа или некоторые противопоказния к нему, не являющиеся противопоказанием к назначению гепарина, служат показанием (при отсутствии собственных противопоказаний) к проведению антикоагулянтной терапии. Ее цель заключается в предупреждении или ограничении тромбоза венечных артерий, а также в профилактике тромбоэмболических осложнений (особенно частых у больных передним инфарктом миокарда, при низком сердечном выбросе, мерцательной аритмии). Для этого на догоспитальном этапе (линейной бригадой) внутривенно болюсно вводится гепарин в дозе 10000-15000 МЕ. Если в условиях стационара не проводится тромболитическая терапия, то переходят на длительную внутривенную инфузию гепарина со скоростью 1000 МЕ/час под контролем активированного частичного тромбопластинового времени. Альтернативой может, по-видимому, служить подкожное введение низкомолекулярного гепарина в "лечебной" дозе. Введение гепарина на догоспитальном этапе не служит препятствием к проведению тромболизиса в условиях стационара.
Несмотря на более высокую безопасность гепаринотерапии по сравнению с системным тромболизисом, в связи со значительно меньшей ее эффективностью ряд противопоказаний к ее проведению имеет значительно более жесткий характер, а некоторые относительные противопоказания к тромболизису оказываются абсолютными для гепаринотерапии. С другой стороны гепарин можно назначать больным с некоторыми противопоказаниями к применению тромболитических средств.
Для решения вопроса о возможности назначения гепарина следует уточнить те же моменты, что и для тромболитичечских средств:
- исключить наличие в анамнезе геморрагического инсульта, операций на головном и спинном мозге;
- убедиться в отсутствии опухоли и язвенной болезни желудка и двенадцатиперстной кишки, инфекционного эндокардита, тяжелого поражения печени и почек;
- исключить подозрение на острый панкреатит, расслаивающую аневризму аорты, острый перикардит с шумом трения перикарда, выслушиваемым в течение нескольких дней(!) (опасность развития гемоперикарда);
- установить отсутствие физикальных признаков или анамнестических указаний на патологию свертывающей системы крови (геморрагические диатезы, болезни крови);
Выяснить, нет ли у больного повышенной чувствительности к гепарину;
- добиться стабилизации повышенного артериального давления на уровне менее 200/120 мм рт. ст.
В). С первых минут инфаркта миокарда всем больным при отсутствии противопоказаний показано назначение малых доз ацетилсалициловой кислоты (аспирина), антитромбоцитарный эффект которой достигает своего максимума уже через 30 минут и своевременное начало применения которой позволяет существенно снизить летальность. Наибольший клинический эффект может быть получен при применении ацетилсалициловой кислоты перед проведением тромболизиса. Доза для первого приема на догоспитальном этапе составляет 160-325 мг, разжевать(!). В дальнейшем, на стационарном этапе, препарат назначается 1 раз в сутки по 100-125 мг.
Для решения вопроса о возможности назначения ацетилсалициловой кислоты имеет значение лишь небольшая часть ограничений для тромболитичечских средств; необходимо уточнить:
Имеются ли у больного эрозивно-язвенные поражения ЖКТ в стадии обострения;
Имелись ли в анамнезе желудочно-кишечные кровотечения;
Нет ли у больного анемии;
- нет ли у больного “аспириновой триады” ( , полипоз носа,
Непереносимость аспирина);
Имеется ли повышенная чувствительность к препарату?
3. Уменьшение работы сердца и потребности миокарда в кислороде
кроме полноценного обезболивания обеспечивается применением
а) вазодилататоров - нитратов,
б) бета-адреноблокаторов и
в) средствами комплексного воздействия - магния сульфата.
А. Внутривенное введение нитратов при остром инфаркте миокарда не только помогает купировать болевой синдром, левожелудочковую недостаточность, артериальную гипертензию, но и уменьшает размеры некроза и летальность. Растворы нитратов для внутривенного введения готовят ex tempore: каждые 10 мг нитроглицерина (например, 10 мл 0,1 % раствора в виде препарата перлинганит) или изосорбида динитрата (например, 10 мл 0,1 % раствора в виде препарата изокет) разводят в 100 мл физиологического раствора (20 мг препарата - в 200 мл физиологического раствора и т.д.); таким образом 1 мл приготовленного раствора содержит 100 мкг, а 1 капля - 5 мкг препарата. Нитраты вводят капельно под постоянным контролем артериального давления и частоты сердечных сокращений с начальной скоростью 5-10 мкг/мин с последующим увеличением скорости на 20 мкг/мин каждые 5 минут до достижения желаемого эффекта или максимальной скорости введения - 400 мкг/мин. Обычно эффект достигается при скорости 50-100 мкг/мин. При отсутствии дозатора приготовленный раствор, содержащий в 1 мл 100 мкг нитрата, вводят при тщательном контроле (см. выше) с начальной скоростью 6-8 капель в минуту, которая при условии стабильной гемодинамики и сохранения болевого синдрома может быть постепенно увеличена вплоть до максимальной скорости - 30 капель в минуту. Введение нитратов проводится как линейными, так и специализированными бригадами и продолжается в стационаре. Продолжительность внутривенного введения нитратов - 24 часа и более; за 2-3 часа до окончания инфузии дается первая доза нитратов перорально. Передозировка нитратов, вызывающая падение сердечного выброса и снижение систолического артериального давления ниже 80 мм рт. ст., может приводить к ухудшению коронарной перфузии и к увеличению размеров инфаркта миокарда.
Для решения вопроса о возможности назначения нитратов необходимо уточнить ряд моментов:
- убедиться, что систолическое артериальное давление выше 90 мм рт. ст. (для короткодействующего нитроглицерина) или выше 100 мм рт. ст (для более продолжительно действующего изосорбида динитрата);
- исключить наличие стеноза устья аорты и гипертрофической кардиомиопатии с обструкцией выносного тракта (аускультативно и по данным ЭКГ), тампонаду сердца (клиническая картина венозного застоя по большому кругу кровообращения при минимальных признаках левожелудочковой недостаточности) и констриктивный перикардит (триада Бека: высокое венозное давление, асцит, “малое тихое сердце”);
- исключить внутричерепную гипертензию и острую церебральную дисциркуляцию (в том числе как проявления инсульта, острой гипертонической энцефалопатии, недавно перенесенной черепно-мозговой травмы);
- исключить возможность провокации нитратами развития синдрома малого выброса вследствие поражения правого желудочка при инфаркте или ишемии правого желудочка, которые могут сопутствовать задней (нижней) локализации инфаркта левого желудочка, или при тромбоэмболии легочной артерии с формированием острого легочного сердца;
- убедиться с помощью пальпаторного обследования в отсутствии высокого внутриглазного давления (при закрытоугольной глаукоме);
- уточнить, нет ли у больного непереносимости нитратов.
Б. Внутривенное введение бета-адреноблокаторов
также как и применение нитратов способствует купированию болевого синдрома; ослабляя симпатические влияния на сердце (эти влияния усилены в первые 48 часов инфаркта миокарда вследствие самого заболевания и в результате реакции на боль) и снижая потребность миокарда в кислороде, они способствуют уменьшению размеров инфаркта миокарда, подавляют желудочковые аритмии, уменьшают риск разрыва миокарда и повышают таким образом выживаемость пациентов. Очень важно, что бета-адреноблокаторы согласно экспериментальным данным позволяют отсрочить гибель ишемизированных кардиомиоцитов (они увеличивают время, в течение которого окажется эффективным тромболизис).
При отсутствии противопоказаний бета-адреноблокаторы назначаются всем больным острым инфарктом миокарда. На догоспитальном этапе показаниями к их внутривенному введению служат для линейной бригады - соответствующие нарушения ритма, а для специализированной - упорный болевой синдром, тахикардия, артериальная гипертензия. В первые 2-4 часа заболевания показано дробное внутривенное введение пропранолола (обзидана) по 1 мг в минуту каждые 3-5 минут под контролем артериального давления, частоты сердечных сокращений и ЭКГ до достижения частоты сердечных сокращений 55-60 уд./мин или до общей дозы 10 мг. При наличии брадикардии, признаков сердечной недостаточности, AV-блокакды и снижении систолического артериального давления менее 100 мм рт. ст. пропранолол не назначается, а при развитии указанных изменений на фоне его применения введение препарата прекращается.
Для решения вопроса о возможности назначения бета-адреноблокаторов необходимо уточнить ряд моментов:
- убедиться в отсутствии острой сердечной недостаточности или недостаточности кровообращения II-III стадии, артериальной гипотензии;
- исключить наличие AV блокады, синоатриальной блокады, синдрома слабости синусового узла, брадикардии (ЧСС менее 55 ударов в минуту);
- исключить наличие бронхиальной астмы и других обструктивных заболеваний дыхательных путей, а также вазомоторного ринита;
- исключить наличие облитерирующих заболеваний сосудов ( или эндартерит, синдром Рейно и др.);
В) Внутривенная инфузия магния сульфата
проводится у больных с доказанной или вероятной гипомагнезиемией или при синдроме удлиненного QT, а также в случае осложнения инфаркта миокарда некоторыми вариантами аритмий. При отсутствии противопоказаний магния сульфат может служить определенной альтернативой применению нитратов и бета-адреноблокаторов, если их введение по какой-то причине невозможно (противопоказания или отсутствие). По результатам ряда исследований он, как и другие средства, уменьшающие работу сердца и потребность миокарда в кислороде, снижает летальность при остром инфаркте миокарда, а также предотвращает развитие фатальных аритмий (в том числе, реперфузионных при проведении системного тромболизиса) и постинфарктной сердечной недостаточности. При лечении острого инфаркта миокарда 1000 мг магния (50 мл 10 %, 25 мл 20 % или 20 мл 25 % раствора сернокислой магнезии) вводятся внутривенно капельно в течение 30 минут в 100 мл изотонического раствора натрия хлорида; в последующем проводится внутривенная капельная инфузия в течение суток со скоростью 100-120 мг магния в час (5-6 мл 10 %, 2,5-3 мл 20 % или 2-2,4 мл 25 % раствора сернокислой магнезии).
Для решения вопроса о показаниях к назначению магния сульфата необходимо уточнить ряд моментов:
- выявить клинические и анамнестические признаки возможной гипомагнезиемии - гиперальдостеронизм (в первую очередь при застойной сердечной недостаточности и стабильной атрериальной гипертензии), гипертиреоз (в том числе ятрогенный), хроническая алкогольная интоксикация, судорожные сокращения мышц, длительное применение диуретиков, глюкокортикоидная терапия;
- диагностировать наличие синдрома удлиненного QT по ЭКГ.
Для решения вопроса о возможности назначения магния сульфата необходимо уточнить ряд моментов:
- убедиться в отсутствии состояний, проявляющихся гипермагнезиемией - почечной недостаточности, диабетического кетоацидоза, гипотиреоза;
- исключить наличие AV блокады, синоаурикулярной блокады, синдрома слабости синусового узла, брадикардии (ЧСС менее 55 ударов в минуту);
Исключить наличие у больного миастении;
- уточнить, нет ли у больного непереносимости препарата.
4. Ограничение размеров инфаркта миокарда
достигается адекватным обезболиванием, восстановлением коронарного кровотока и уменьшением работы сердца и потребности миокарда в кислороде.
Этой же цели служит оксигенотерапия, показанная при остром инфаркте миокарда всем больным в связи с частым развитием гипоксемии даже при неосложненном течении заболевания. Ингаляция увлажненного кислорода, проводящаяся, если это не причиняет чрезмерных неудобств, с помощью маски или через носовой катетер со скоростью 4-6 л/мин, целесообразна в течение первых 24-48 часов заболевания (начинается на догоспитальном этапе и продолжается в стационаре).
5. Лечение и профилактика осложнений инфаркта миокарда.
Все перечисленные мероприятия вместе с обеспечением физического и психического покоя, госпитализацией на носилках служат профилактике осложнений острого инфаркта миокарда. Лечение же в случае их развития проводится дифференцированно в зависимости от варианта осложнений: отек легких, кардиогеннй шок, нарушения сердечного ритма и проводимости, а также затянувшийся или рецидивирующий болевой приступ.
1). При острой левожелудочковой недостаточности с развитием сердечной астмы или отека легких одновременно с введением наркотических анальгетиков и нитроглицерина внутривенно струйно вводят 40-120 мг (4-12 мл) раствора фуросемида (лазикса), максимальная доза на догоспитальном этапе - 200 мг.
2). Основой лечения кардиогенного шока служит ограничение зоны повреждения и увеличение объёма функционирующего миокарда путём улучшения кровоснабжения его ишемизированных участков, для чего проводится системный тромболизис.
Аритмический шок требует немедленного восстановления адекватного ритма путем проведения электроимпульсной терапии, электрокардиостимуляция, при невозможности их проведения показана медикаментозная терапия (см. далее).
Рефлекторный шок купируется после проведения адекватной анальгезии; при исходной брадикардии опиоидные анальгетики нужно сочетать с атропином в дозе 0,5 мг.
Истинный кардиогенный шок (гипокинетический тип гемодинамики ) служит показанием к в/в капельному введению негликозидных кардиотонических (положительных инотропных) средств - допамина, добутамина, норэпинефрина. Этому должна предшествовать коррекция гиповолемии. При отсутствии признаков застойной левожелудочковой недостаточности ОЦК корригируется струйным введением 0,9% раствора натрия хлорида в объёме до 200 мл за 10 мин с повторным введением той же дозы при отсутствии эффекта или осложнений.
Допамин в дозе 1-5 мкг/кг/мин оказывает преимущественно вазодилатирующее действие, 5-15 мкг/кг/мин - вазодилатирующее и положительное инотропное (и хронотропное) действие, 15-25 мкг/кг/мин - положительное инотропное (и хронотропное) и периферическое вазоконстриктивное действие. Начальная доза составляет 2-5 мкг/кг/мин с постепенным увеличением до оптимальной.
Добутамин в отличие от допамина не вызывает вазодилатацию, но обладает мощным положительным инотропным эффектом и менее выраженными увеличением ЧСС и аритмогенном эффектом. Препарат назначается в дозе 2,5 мкг/кг/мин с увеличением каждые 15-30 мин на 2,5 мкг/кг/мин до получения эффекта, побочного действия или достижения дозы 15 мкг/кг/мин.
Комбинация допамина с добутамином в максимально переносимых дозах используется при отсутствии эффекта от максимальной дозы одного из них или при невозможности использования максимальной дозы одного препарата из-за появления побочных эффектов (синусовая тахикардия более 140 в минуту или желудочковая аритмия).
Комбинация допамина или добутамина с норэпинефрином, назначаемым в дозе 8 мкг/мин.
Норэпинефрин (норадреналин) в качестве монотерапии применяется при невозможности использовать другие прессорные амины. Назначается в дозе, не превышающей 16 мкг/мин, в обязательном сочетании с инфузией нитроглицерина или изосорбида динитрата со скоростью 5-200 мкг/мин.
3). Желудочковая экстрасистолия в острой стадии инфаркта миокарда может быть предвестником фибрилляции желудочков. Препарат выбора для лечения желудочковых нарушений ритма - лидокаин - вводится внутривенно болюсом из расчета 1 мг/кг массы с последующей капельной инфузией 2-4 мг/мин. Не рекомендуется применявшееся ранее профилактическое назначение лидокаина всем больным острым инфарктом миокарда (препарат увеличивает летальность вследствие асистолии). Больным с застойной сердечной недостаточностью, заболеваниями печени, вводят в дозе, сниженной вдвое.
При желудочковой тахикардии, трепетании предсердий и мерцательной аритмии с высокой ЧСС и нестабильной гемодинамикой средством выбора является дефибрилляция. При мерцательной тахиаритмии и стабильной гемодинамике используют (анаприлин, обзидан) для урежения ЧСС.
При развитии атрио-вентрикулярной блокады II-III степени внутривенно вводят 1 мл 0,1% раствора атропина, при неэффективности пробной терапии атропином и появлении обмороков (приступов Морганьи-Эдемса-Стокса) показана временная электрокардиостимуляция.
ЧАСТО ВСТРЕЧАЮЩИЕСЯ ОШИБКИ ТЕРАПИИ.
Высокая летальность в первые часы и сутки инфаркта миокарда обусловливает необходимость назначения адекватной медикаментозной терапии, начиная с первых минут заболевания. Потеря времени значительно ухудшает прогноз.
А. Ошибки, обусловленные устаревшими рекомендациями, частично сохраняющимися и в некоторых современных стандартах оказания медицинской помощи на догоспитальном этапе.
Наиболее распространенной ошибкой является использование трехступенчатой схемы обезболивания: при отсутствии эффекта от сублингвального приема нитроглицерина переход к наркотическим анальгетикам осуществляется только после безуспешной попытки купировать болевой синдром с помощью комбинации ненаркотического анальгетика (метамизола натрия - анальгина) с антигистаминным препаратом (дифенидрамином - димедролом). Между тем, потеря времени при использовании такой комбинации, которая, во-первых, как правило не позволяет получить полной анальгезии, а во-вторых, не способна в отличие от наркотических анальгетиков обеспечить гемодинамическую разгрузку сердца (главную цель обезболивания) и уменьшить потребность миокарда в кислороде, приводит к усугублению состояния и ухудшению прогноза.
Значительно реже, но все еще применяются миотропные спазмолитики (как исключение используется рекомендовавшийся ранее папаверин, на смену которому пришел дротаверин - но-шпа), не улучшающие перфузию пораженной зоны, но повышающие потребность миокарда в кислороде.
Нецелесообразно применение атропина для профилактики (это не касается купирования) вагомиметических эффектов морфина (тошнота, рвота, влияние на сердечный ритм и артериальное давление), поскольку он может способствовать увеличению работы сердца.
Рекомендующееся профилактическое назначение лидокаина всем больным острым инфарктом миокарда без учета реальной ситуации, предупреждая развитие фибрилляции желудочков, может значительно увеличивать летальность вследствие наступления асистолии.
Б. Ошибки, обусловленные другими причинами.
Весьма часто в целях обезболивания при ангинозном статусе неоправданно используется комбинированный препарат метамизол натрия с фенпиверином бромидом и питофеноном гидрохлоридом (баралгин, спазмалгин, спазган и т. д.) или трамадол (трамал), практически не влияющие на работу сердца и потребление кислорода миокардом, а потому не показанные в этом случае (см. выше).
Крайне опасно при инфаркте миокарда применение в качестве антиагрегантного средства и “коронаролитика” дипирадамола (курантила), значительно повышающего потребность миокарда в кислороде.
Весьма распространенной ошибкой является назначение калия и магния аспартата (аспаркама, панангина), не влияющего ни на внешнюю работу сердца, ни на потребление миокардом кислорода, ни на коронарный кровоток и т.д.
ПОКАЗАНИЯ К ГОСПИТАЛИЗАЦИИ.
Острый инфаркт миокарда является прямым показанием к госпитализации в отделение (блок) интенсивной терапии или кардиореанимации. Транспортировка осуществляется на носилках.
На чтение 6 мин. Просмотров 773
(ИМ) — патология системы сердца и сосудов, которую пациенты часто путают со стенокардией. Однако в отличие от последнего состояния, ИМ при несвоевременном оказании квалифицированной помощи приводит к тяжелым последствиям: инвалидизации пациента или даже летальному исходу.
ЭКГ при инфаркте миокарда — методика, позволяющая обнаружить признаки угрожающего жизни состояния еще на начальных стадиях.
Так же как и сам инфаркт, изменения на ЭКГ при данной нозологии можно классифицировать в зависимости от стадии ишемии, размера пораженного очага и его локализации.
В зависимости от стадии
Кардиограмма при инфаркте позволяет выявить изменения строгого временного характера. Электрокардиографическая кривая различается в зависимости от стадии заболевания и проявления степени ишемии и некроза.
Стадии инфаркта включают в себя следующие этапы.
Как часто Вы сдаете анализ крови?
Poll Options are limited because JavaScript is disabled in your browser.
Только по назначению лечащего врача 30%, 661 голос
Один раз в год и считаю этого достаточно 17%, 371 голос
Как минимум два раза в год 15%, 322 голоса
Чаще чем два раза в год но меньше шести раз 11%, 248 голосов
Я слежу за своим здоровьем и сдаю раз в месяц 7%, 151 голос
Боюсь эту процедуру и стараюсь не сдавать 4%, 96 голосов
21.10.2019
Первые часы сопровождаются различной степенью повреждения сердечной мышцы вследствие ишемии — острейшая фаза. Для нее характерно:
- кривая монофазного типа, возникшая из-за слияния сегмента ST c высоким зубцом T, — это главный признак ЭКГ;
- наличие или отсутствие зубца Q, вызванного некротическими изменениями в ткани миокарда;
- исчезновение зубца R (наблюдается в тех случаях, когда появляется глубокий Q на кардиограмме).
При острой стадии, продолжительность которой колеблется от 2 до 10 суток, наблюдается:
- формирование отрицательного Т или полное его отсутствие;
- большое возвышение сегмента ST по отношению к изолинии, которая располагается над областью нарушения кровообращения;
- Q становится глубже вплоть до появления QT-комплекса.
В подострой (30-60 сутки) наблюдаются следующие показатели кардиограммы:
- зубец T ниже изолинии, амплитуда его увеличивается за счет расширения обескровленной зоны. Нормализуется зубец только во второй половине подострой стадии;
- снижение ST сегмента вплоть до окончания подострой стадии;
- для первых 3 стадий характерны важные особенности электрокардиографической кривой: подъем ST в отведениях, которые соответствуют зоне повреждения и, наоборот, снижение в противоположных ишемическим изменениям участках сердечной мышцы.

Для рубцовой стадии (длительность составляет 7-90 дней) характерно:
- достижение зубцом T изолинии либо положительное его расположение;
- если при острой стадии появляется патологический Q, в рубцовой он сохраняется;
- R становится выше.
В зависимости от размера очага
Электрокардиограмма также может различаться в зависимости от того, насколько обширную зону волокон сердечной мышцы затронуло нарушение кровотока в сосудах.
При ишемии в крупных сосудистых стволах поражение носит обширный характер, тогда как мини-инфаркты сопровождаются нарушением кровоснабжения концевыми артериальными ветвями.
Определить инфаркт на ЭКГ можно по признакам, которые зависят от его размера:
- Крупноочаговый трансмуральный (при данном типе патологии затронута вся толща кардиальной стенки):
- отсутствует зубец R;
- Q расширенный и глубокий;
- слияние ST с зубцом T над зоной ишемии
- Т ниже изолинии в подострой стадии.
- Крупноочаговый субэпикардиальный (локализация инфаркта в зоне рядом с эпикардом):
- наличие уменьшенного зубца R;
- глубокий и широкий зубец Q, который переходит в высокий ST;
- зубец T отрицательный в подострой стадии.
- Мелкоочаговый интрамуральный инфаркт (характерна локализация во внутренних слоях кардиальной мышцы).
- не затронуты зубцы R и Q;
- изменения в сегменте ST отсутствуют;
- на протяжении 14 дней сохраняется T, расположенный ниже изолинии.
- Мелкоочаговый субэндокардиальный:
- патология R и Q не выявляется;
- ST на 0,02 mV и более опускается ниже изолинии;
- зубец T сглажен.
Важная информация: Какие препараты принимать после инфаркта миокарда

При разном расположении инфаркта
Локализация зоны ишемии — еще один фактор, который влияет на ЭКГ признаки инфаркта миокарда.
Расшифровка инфаркта миокарда на ЭКГ осуществляется в 12 отведениях, каждое из которых отвечает за соответствующий участок сердечной мышцы.
Стандартные отведения:
- І — отображает информацию об изменениях, локализованных в передней и боковой части левого желудочка;
- ІІІ — позволяет оценить состояние задней части диафрагмальной поверхности сердца;
- ІІ отведение используется с целью подтверждения данных, полученных при оценке І или ІІІ отведения.
Усиленные отведения:
- aVL (усиленное от левой руки) — позволяет оценить изменения на боковой стенке левого желудочка;
- aVF (усиленное от правой ноги) — задняя часть диафрагмальной поверхности;
- aVR (усиленное от правой руки) — считается малоинформативным, однако может использоваться для оценки инфарктных изменений в межжелудочковой перегородке и нижне-боковых отделах левого желудочка.
Грудные отведения:
- V1, V2 — изменения в межжелудочковой перегородке;
- V3 — передняя стенка;
- V4 — верхушечная локализация инфаркта;
- V5, V6 — боковая часть левого желудочка.
Передний или переднеперегородочный
При такой локализации поражения на кардиограмме изменения оценивают следующим образом:
- в I,II стандартном и aVL отведениях наблюдается зубец Q и единый с зубцом Т сегмент ST;
- в III стандартном и aVF отведениях — переход ST в расположенный ниже линии Т-зубец;
- в 1,2,3 грудных, а также при переходе на 4 грудное — отсутствие R и расположение ST выше линии на 0,2-0,3 см и более;
- отведения aVR и 4,5,6 грудные покажут следующие изменения: зубец Т уплощен, ST смещен вниз.
Боковой
ЭКГ при инфаркте с боковой локализацией сопровождается расширением и углублением Q-зубца, повышением ST и соединением этого сегмента с Т-зубцом. Эти признаки наблюдаются в III стандартном, 5,6 грудном и aVF отведениях.
Инфаркт на ЭКГ при диафрагмальной локализации имеет признаки:
- II, III и aVF отведения: широкий Q, положительный Т, соединенный с высоким ST;
- I отведение: опустившийся ниже линии ST;
- в некоторых случаях во всех грудных отведениях видны изменения зубца Т в виде отрицательной деформации и снижение ST.
Межжелудочковой перегородки
Поражение межжелудочковой перегородки инфарктом на ЭКГ проявляется углублением Q, подъемом Т и ST в отведениях, передающих информацию о состоянии передней части перегородки (I, aVL, 1,2 грудное). При ишемии в задней части перегородки (1 и 2 грудные отведения) видны: увеличенный зубец R, атриовентрикулярная блокада разных степеней и небольшое смещение ниже изолинии ST сегмента.

Передний субэндокардиальный
Этому виду инфаркта характерны изменения на ЭКГ:
- в I, aVL и 1-4 грудных отведениях — зубец Т положительный, высота его больше, чем у R;
- II, III стандартные — плавное снижение ST, отрицательное расположение зубца Т, низкий R;
- 5 и 6 грудные — разделение Т на отрицательную и положительную части.
Задний субэндокардиальный
При задней субэндокардиальной локализации признаки инфаркта миокарда на ЭКГ во II, III, aVF и 5, 6 грудном отведениях: зубец R уменьшается, Т становится положительным, а позже ST начинает опускаться.
Инфаркт правого желудочка
Т.к. у правого и левого желудочков общий источник кровоснабжения (коронарные артерии), при инфаркте в правой половине возникают изменения и в переднем отделе левого желудочка.
Диагностика с использованием электродов редко позволяет эффективно распознать правожелудочковый инфаркт даже с использованием дополнительных электродов. При этом типе нарушения кровообращения сердца показателям ЭКГ предпочтительна ультрасонография.
Несмотря на информативность метода, кардиограмма не является единственным тестом, на данные которого стоит опираться при диагностике инфаркта. Наряду с изменениями на кардиографической кривой учитываются клинические симптомы и показатели уровня кардиоспецифических ферментов: МВ-КФК, КФК, ЛДГ и др. Только наличие 2 и более признаков дает основание с точностью поставить диагноз.
На ЭКГ проявляется в зависимости от стадии развития. Эта процедура проводится всегда для определения локализации и размера очага некроза. Это надежное исследование, расшифровка которого помогает заметить любые патологические изменения в сердце.
Что такое ЭКГ
Электрокардиограмма - это диагностическая методика, которая фиксирует сбои в функционировании сердца. Процедура проводится с помощью электрокардиографа. Аппарат предоставляет изображение в виде кривой, которое свидетельствует о прохождении электрических импульсов.
Это безопасная диагностическая методика, разрешена для проведения во время беременности и в детском возрасте.
С помощью кардиограммы определяют:
- в каком состоянии структура, способствующая сокращению миокарда;
- частоту сокращений сердца и его ритм;
- работу проводящих путей;
- оценивают качество снабжения сердечной мышцы через коронарные сосуды;
- выявляют наличие рубцов;
- патологии сердца.
Для более точной информации о состоянии органа могут использовать суточное мониторирование, ЭКГ с нагрузкой, чрезпищеводное ЭКГ. Благодаря этим процедурам можно своевременно обнаружить развитие патологических процессов.
