Milyen generációs Tavegil a gyógyszer. Antihisztaminok - generációk, hatáselvek, gyógyszerek áttekintése
A hisztamin kórélettana ésH 1- hisztamin receptorok
A hisztamin és hatásai a H 1 receptorokon keresztül közvetítettek
Emberben a H 1 receptorok stimulálása a simaizom tónusának növekedéséhez, az érpermeabilitás növekedéséhez, viszketéshez, az atrioventrikuláris vezetés lassulásához, tachycardiához, a légutakat beidegző vagus ideg ágainak aktiválódásához, a cGMP szint emelkedéséhez, a cGMP szint növekedéséhez vezet. a prosztaglandinok képződésében stb. táblázatban. A 19-1. ábra a lokalizációt mutatja H 1 receptorok és a rajtuk keresztül közvetített hisztamin hatásai.
19-1. táblázat. Lokalizáció H 1 receptorok és a rajtuk keresztül közvetített hisztamin hatásai
A hisztamin szerepe az allergia patogenezisében
A hisztamin vezető szerepet játszik az atópiás szindróma kialakulásában. Az IgE által közvetített allergiás reakciókban a hízósejtekből nagy mennyiségű hisztamin kerül a szövetekbe, ami a H 1 receptorokra hatva az alábbi hatások fellépését okozza.
A nagy erek, a hörgők és a belek simaizomzatában a H1 receptorok aktiválódása megváltoztatja a Gp fehérje konformációját, ami viszont a foszfolipáz C aktiválódásához vezet, amely katalizálja az inozit-difoszfát hidrolízisét inozit-trifoszfáttá. és diacil-glicerinek. Az inozitol-trifoszfát koncentrációjának növekedése a kalciumcsatornák megnyitásához vezet az ER-ben („kalcium depó”), ami a kalcium felszabadulását okozza a citoplazmában, és növeli a sejten belüli koncentrációját. Ez a miozin könnyű láncok kalcium/kalmodulin-függő kinázának aktiválásához, és ennek megfelelően a simaizomsejtek összehúzódásához vezet. A kísérletben a hisztamin a légcső simaizmainak kétfázisú összehúzódását okozza, amely egy gyors fázisösszehúzódásból és egy lassú tónusos komponensből áll. Kísérletek kimutatták, hogy ezen simaizmok összehúzódásának gyors fázisa az intracelluláris kalciumtól függ, míg a lassú fázis az extracelluláris kalcium lassú, kalcium-antagonisták által feloldott kalciumcsatornákon keresztül történő bejutásától függ. A H 1 receptorokon keresztül hatva a hisztamin a légutak simaizmainak összehúzódását okozza, beleértve a hörgőket is. A légutak felső szakaszain több hisztamin H1 receptor található, mint az alsókban, ami elengedhetetlen a hörgőgörcs súlyosságának mértékéhez a hörgőkben a hisztamin ezen receptorokkal való kölcsönhatása során. A hisztamin a légúti simaizomzatra gyakorolt közvetlen hatás eredményeként hörgőelzáródást vált ki, és reagál a hisztamin H 1 receptorokkal. Emellett a H 1 receptorokon keresztül a hisztamin fokozza a légutakban a folyadék- és elektrolitszekréciót, valamint fokozott nyálkatermelést és légúti ödémát okoz. A bronchiális asztmában szenvedő betegek 100-szor érzékenyebbek a hisztaminra, mint az egészségesek, amikor hisztamin provokációs tesztet végeznek.
A kiserek endotéliumában (posztkapilláris venulák) a hisztamin értágító hatása a H 1 receptorokon keresztül közvetítődik a reagin típusú allergiás reakciókban (a venulák simaizomsejtjeinek H 2 receptorain keresztül, az adenilát cikláz út mentén). A H 1 receptorok aktiválása (a foszfolipáz útvonalon keresztül) az intracelluláris kalciumszint növekedéséhez vezet, ami a diacilglicerinnel együtt aktiválja a foszfolipáz A 2-t, ami a következő hatásokat okozza.
Az endothel-relaxáló faktor lokális felszabadulása. Bejut a szomszédos simaizomsejtekbe, és aktiválja a guanilát-ciklázt. Ennek eredményeként megnő a cGMP-dependens proteinkinázt aktiváló cGMP koncentrációja, ami az intracelluláris kalcium csökkenéséhez vezet. A kalciumszint egyidejű csökkenésével és a cGMP szintjének emelkedésével a posztkapilláris venulák simaizomsejtjei ellazulnak, ami ödéma és erythema kialakulásához vezet.
A foszfolipáz A2 aktiválásakor a prosztaglandinok, elsősorban a prosztaciklin értágító szintézise fokozódik, ami szintén hozzájárul az ödéma és az erythema kialakulásához.
Az antihisztamin gyógyszerek osztályozása
Az antihisztaminok (hisztamin H1 receptor blokkolók) többféle besorolása létezik, bár egyik sem tekinthető általánosan elfogadottnak. Az egyik legnépszerűbb besorolás szerint az antihisztaminokat a létrehozásuk időpontja szerint I és II generációs gyógyszerekre osztják. Az első generációs gyógyszereket általában nyugtatóknak is nevezik (a domináns mellékhatás szerint), ellentétben a második generációs, nem nyugtató szerekkel. Az első generációs antihisztaminok a következők: difenhidramin (difenhidramin*), prometazin (diprazin*, pipolfen*), klemasztin, kloropiramin (suprastin*), hifenadin (fenkarol*), szekvifenadin (bikarfen*). Második generációs antihisztaminok: terfenadin*, asztemizol*, cetirizin, loratadin, ebasztin, ciproheptadin, oxatomid*9, azelasztin, akrivasztin, mebhidrolin, dimetindén.
Jelenleg az antihisztaminok harmadik generációját szokás elkülöníteni. Alapvetően új gyógyszereket tartalmaz - aktív metabolitokat, amelyeket a magas antihisztamin aktivitás mellett a nyugtató hatás hiánya és a második generációs gyógyszerekre jellemző kardiotoxikus hatás jellemez. Az antihisztaminok harmadik generációjába tartozik a fexofenadin (telfast*), dezloratadin.
Ezenkívül a kémiai szerkezet szerint az antihisztaminok több csoportra oszthatók (etanol-aminok, etilén-diaminok, alkil-aminok, alfakarbolin származékai, kinuklidin, fenotiazin *, piperazin * és piperidin *).
Az antihisztamin gyógyszerek hatásmechanizmusa és fő farmakodinámiás hatásai
Az alkalmazott antihisztaminok többsége specifikus farmakológiai tulajdonságokkal rendelkezik, ami külön csoportként jellemzi őket. Ide tartoznak a következő hatások: viszketéscsillapító, dekongesztáns, görcsoldó, antikolinerg, antiszerotonin, nyugtató és helyi érzéstelenítő, valamint a hisztamin által kiváltott bronchospasmus megelőzése.
Az antihisztaminok hisztamin H 1 receptor antagonisták, és ezekhez a receptorokhoz való affinitásuk sokkal kisebb, mint a hisztamin (19-2. táblázat). Éppen ezért ezek a gyógyszerek nem képesek kiszorítani a receptorhoz kapcsolódó hisztamint, csak a nem foglalt vagy felszabaduló receptorokat blokkolják.
19-2. táblázat. Az antihisztamin gyógyszerek összehasonlító hatékonysága a blokád mértéke szerint H 1- hisztamin receptorok
 Ennek megfelelően blokkolók H 1 A hisztamin receptorok a leghatékonyabbak az azonnali allergiás reakciók megelőzésében, kialakult reakció esetén pedig megakadályozzák a hisztamin újabb adagjainak felszabadulását. Az antihisztaminok kötődése a receptorokhoz reverzibilis, és a blokkolt receptorok száma egyenesen arányos a hatóanyag koncentrációjával a receptor helyén.
Ennek megfelelően blokkolók H 1 A hisztamin receptorok a leghatékonyabbak az azonnali allergiás reakciók megelőzésében, kialakult reakció esetén pedig megakadályozzák a hisztamin újabb adagjainak felszabadulását. Az antihisztaminok kötődése a receptorokhoz reverzibilis, és a blokkolt receptorok száma egyenesen arányos a hatóanyag koncentrációjával a receptor helyén.
Az antihisztaminok molekuláris hatásmechanizmusa egy sémaként ábrázolható: a H 1 receptor blokkolása - a foszfoinozitid út blokkolása a sejtben - a hisztamin hatásának blokkolása. A gyógyszereknek a hisztamin H 1 receptorhoz való kötődése a receptor „blokádjához” vezet, pl. megakadályozza a hisztamin kötődését a receptorhoz és egy kaszkád elindítását a sejtben a foszfoinozitid útvonalon. Így egy antihisztamin gyógyszer kötődése a receptorhoz a foszfolipáz C aktiválódásának lelassulását okozza, ami az inozit-trifoszfát és a diacil-glicerin képződésének csökkenéséhez vezet a foszfatidil-inozitolból, ennek eredményeként lelassul a kalcium felszabadulása az intracelluláris depókban. . A különböző sejttípusokban az intracelluláris organellumokból a citoplazmába történő kalcium felszabadulás csökkenése a hisztamin hatását közvetítő aktivált enzimek arányának csökkenéséhez vezet ezekben a sejtekben. A hörgők simaizomzatában (valamint a gyomor-bél traktusban és a nagy erekben) a miozin könnyű láncok kalcium-kalmodulin-függő kinázának aktiválódása lelassul. Ez megakadályozza a hisztamin okozta simaizom-összehúzódást, különösen a bronchiális asztmában szenvedő betegeknél. A bronchiális asztmában azonban a hisztamin koncentrációja a tüdőszövetben olyan magas, hogy a modern H1-blokkolók ezen a mechanizmuson keresztül nem képesek blokkolni a hisztamin hörgőkre gyakorolt hatását. Az összes posztkapilláris venula endothel sejtjeiben az antihisztaminok megakadályozzák a hisztamin értágító hatását (közvetlenül és prosztaglandinokon keresztül) lokális és generalizált allergiás reakciókban (a hisztamin a simaizomsejtek hisztamin H 2 receptorain keresztül is hat
venule az adenilát-cikláz útvonalon keresztül). A hisztamin H 1 receptorok blokkolása ezekben a sejtekben megakadályozza az intracelluláris kalciumszint emelkedését, végső soron lelassítja a foszfolipáz A2 aktiválódását, ami a következő hatások kialakulásához vezet:
Lelassítja az endothel-relaxáló faktor helyi felszabadulását, amely behatol a szomszédos simaizomsejtekbe és aktiválja a guanilát-ciklázt. A guanilát-cikláz aktiváció gátlása csökkenti a cGMP koncentrációját, majd az aktivált cGMP-függő protein kináz frakciója csökken, ami megakadályozza a kalciumszint csökkenését. Ugyanakkor a kalcium és a cGMP szintjének normalizálása megakadályozza a posztkapilláris venulák simaizomsejtjeinek ellazulását, azaz megakadályozza a hisztamin okozta ödéma és bőrpír kialakulását;
A foszfolipáz A2 aktivált frakciójának csökkenése és a prosztaglandinok (főleg prosztaciklin) szintézisének csökkenése, az értágulás blokkolva van, ami megakadályozza a hisztamin által okozott ödéma és erythema előfordulását a második hatásmechanizmussal ezeken a sejteken.
Az antihisztamin gyógyszerek hatásmechanizmusa alapján ezeket a gyógyszereket fel kell írni a reagin típusú allergiás reakciók megelőzésére. Ezeknek a gyógyszereknek a kijelölése kialakult allergiás reakció esetén kevésbé hatékony, mivel nem szüntetik meg a kialakult allergia tüneteit, hanem megakadályozzák azok előfordulását. A hisztamin H1-receptor blokkolók megakadályozzák a hörgők simaizmainak reakcióját a hisztaminra, csökkentik a viszketést, valamint megakadályozzák a kis erek hisztamin által közvetített tágulását és permeabilitását.
Az antihisztamin gyógyszerek farmakokinetikája
A hisztamin első generációs H 1 -receptor blokkolóinak farmakokinetikája alapvetően eltér a második generációs gyógyszerek farmakokinetikájától (19-3. táblázat).
Az első generációs antihisztaminok behatolása a BBB-n keresztül kifejezett nyugtató hatáshoz vezet, amelyet e gyógyszercsoport jelentős hátrányának tekintenek, és jelentősen korlátozza alkalmazásukat.
A második generációs antihisztaminok viszonylag hidrofilek, ezért nem hatolnak be a BBB-be, és ezért nem okoznak nyugtató hatást. Ismeretes, hogy az asztemizol* 80%-a az utolsó adag beadása után 14 nappal, a terfenadin* pedig 12 nappal később ürül ki.
A difenhidramin kifejezett ionizációja fiziológiás pH-értékeken és aktív, nem specifikus kölcsönhatás a szérummal
Az orális albumin a különböző szövetekben található H1-hisztamin receptorokra fejti ki hatását, ami ennek a gyógyszernek meglehetősen kifejezett mellékhatásaihoz vezet. A vérplazmában a gyógyszer maximális koncentrációját a beadás után 4 órával határozzák meg, és 75-90 ng / l (50 mg-os dózisban). A felezési idő 7 óra.
A klemasztin csúcskoncentrációja 3-5 órával az egyszeri 2 mg-os orális adag bevétele után alakul ki. A felezési idő 4-6 óra.
A terfenadin* szájon át bevéve gyorsan felszívódik. A májban metabolizálódik. A szövetekben a maximális koncentrációt a gyógyszer bevétele után 0,5-1-2 órával határozzák meg, a felezési idő a
A változatlan asztemizol* maximális szintje a gyógyszer bevétele után 1-4 órán belül figyelhető meg. Az étkezés 60%-kal csökkenti az asztemizol* felszívódását. A hatóanyag csúcskoncentrációja a vérben egyszeri szájon át történő bevétel esetén 1 óra után következik be, felezési ideje 104 óra, aktív metabolitjai a hidroxiasztemizol és a norastemizol. Az Astemizol * átjut a placentán, kis mennyiségben - az anyatejbe.
Az oxatomid * maximális koncentrációját a vérben a bevétel után 2-4 órával határozzák meg. A felezési idő 32-48 óra, a fő metabolikus út az aromás hidroxilezés és a nitrogén oxidatív dealkilezése. A felszívódott gyógyszer 76%-a a plazmaalbuminhoz kötődik, 5-15%-a kiválasztódik az anyatejbe.
19-3. táblázat. Egyes antihisztamin gyógyszerek farmakokinetikai paraméterei
 A cetirizin maximális szintjét a vérben (0,3 μg / ml) 30-60 perccel a gyógyszer 10 mg-os dózisának bevétele után határozzák meg. Vese
A cetirizin maximális szintjét a vérben (0,3 μg / ml) 30-60 perccel a gyógyszer 10 mg-os dózisának bevétele után határozzák meg. Vese
a cetirizin clearance-e 30 mg/perc, felezési ideje kb. 9 óra A gyógyszer stabilan kapcsolódik a vérfehérjékhez.
Az akrivasztin plazma csúcskoncentrációja a beadás után 1,4-2 órával érhető el. A felezési idő 1,5-1,7 óra A gyógyszer kétharmada változatlan formában ürül a vesén keresztül.
A loratadin jól felszívódik a gyomor-bél traktusban, és 15 perc elteltével meghatározza a vérplazmában. Az étel nem befolyásolja a gyógyszerek felszívódásának mértékét. A gyógyszer felezési ideje 24 óra.
1. generációs antihisztaminok
Az első generációs hisztamin H 1 -receptorok blokkolóira néhány jellemző jellemző.
nyugtató hatású. A legtöbb első generációs antihisztamin, amely könnyen oldódik lipidekben, jól áthatol a BBB-n és kötődik az agy H1 receptoraihoz. Úgy tűnik, a nyugtató hatás a központi szerotonin és az m-kolinerg receptorok blokkolásával alakul ki. A nyugtató hatás mértéke a közepestől a súlyosig változik, és alkohollal és pszichotróp szerekkel kombinálva fokozódik. E csoportba tartozó egyes gyógyszereket altatóként (doxilamin) használnak. Ritkán szedáció helyett pszichomotoros agitáció lép fel (gyakrabban közepes terápiás dózisokban gyermekeknél és nagy toxikus dózisokban felnőtteknél). A gyógyszerek nyugtató hatása miatt odafigyelést igénylő munkaidőben nem alkalmazhatók. Az első generációs hisztamin H 1 -receptorok összes blokkolója fokozza a nyugtató és hipnotikus gyógyszerek, a kábító és nem kábító fájdalomcsillapítók, a monoamin-oxidáz inhibitorok és az alkohol hatását.
szorongásoldó hatás, a hidroxizinre jellemző. Ez a hatás valószínűleg annak köszönhető, hogy a hidroxizin elnyomja az agy kéreg alatti képződményeinek egyes részeinek aktivitását.
atropinszerű hatás. Ez a hatás az m-kolinerg receptorok blokkolásával jár, ami leginkább az etanol-aminokra és az etilén-diaminokra jellemző. Szájszárazság, vizeletvisszatartás, székrekedés, tachycardia és homályos látás jellemzi. Nem allergiás rhinitisben ezeknek a gyógyszereknek a hatékonysága az m-kolinerg receptorok blokkolása miatt nő. Azonban lehetséges a hörgőelzáródás fokozása a köpet viszkozitásának növekedése miatt, ami veszélyes bronchiális asztmában. A hisztamin I. generációs H 1 -receptorok blokkolói súlyosbíthatják a glaukómát és akut vizeletretenciót okozhatnak prosztata adenomában.
Antiemetikus és vérnyomáscsökkentő hatás. Ezek a hatások összefüggésbe hozhatók ezen gyógyszerek központi m-antikolinerg hatásával is. difenhidramin, prometazin, ciklizin*, mekli-
zine * csökkenti a vesztibuláris receptorok ingerlését és gátolja a labirintus működését, ezért utazási betegség esetén is használható.
A hisztamin H 1 -receptorainak egyes blokkolói csökkentik a parkinsonizmus tüneteit, ami a központi m-kolinerg receptorok blokádjának köszönhető.
Köhögéscsillapító hatás. Legjellemzőbb a difenhidraminra, amely a medulla oblongata köhögési központjára gyakorolt közvetlen hatásnak köszönhető.
Antiszerotonin hatás. A ciproheptadin rendelkezik a legnagyobb mértékben, ezért migrénre használják.
Az 1 adrenalin receptorok perifériás értágulattal járó blokkolásának hatása különösen jellemző a fenotiazin sorozat gyógyszereire. Ez a vérnyomás átmeneti csökkenéséhez vezethet.
Helyi érzéstelenítő hatás jellemző a legtöbb gyógyszer ebben a csoportban. A difenhidramin és a prometazin helyi érzéstelenítő hatása erősebb, mint a novokain*.
Tachyphylaxis- az antihisztamin hatás csökkenése hosszú távú használat esetén, megerősítve a 2-3 hetente váltakozó gyógyszerek szükségességét.
A hisztamin I generációs H1-receptor blokkolók farmakodinámiája
Az első generációs hisztamin H 1 -receptorok összes blokkolója lipofil, és a hisztamin H 1 -receptorai mellett az m-kolinerg receptorokat és a szerotonin receptorokat is blokkolja.
A hisztamin receptor blokkolók felírásakor figyelembe kell venni az allergiás folyamat fázisát. A hisztamin H1 receptor blokkolókat elsősorban a patogenetikai elváltozások megelőzésére kell alkalmazni abban az esetben, ha a páciens állítólagos találkozása van allergénnel.
A hisztamin I generációs H 1 -receptorok blokkolásai nem befolyásolják a hisztamin szintézisét. Nagy koncentrációban ezek a gyógyszerek képesek a hízósejtek degranulációját és hisztamin felszabadulását okozni belőlük. A hisztamin H1-receptor-blokkolói hatékonyabban akadályozzák meg a hisztamin hatását, mint a hatás következményeit. Ezek a gyógyszerek gátolják a hörgők simaizomzatának hisztaminra adott válaszát, csökkentik a viszketést, megakadályozzák, hogy a hisztamin fokozza az értágulatot és növelje permeabilitását, valamint csökkenti az endokrin mirigyek szekrécióját. Bebizonyosodott, hogy az 1. generációs H 1 -receptor-blokkolók a hisztamin közvetlen hörgőtágító hatásúak, és ami a legfontosabb, megakadályozzák a hisztamin felszabadulását a hízósejtekből és a vér bazofiljeiből, ami e gyógyszerek alkalmazásának alapja. .
megelőző intézkedésként. Terápiás dózisban nem befolyásolják jelentősen a szív- és érrendszert. Kényszerített intravénás beadással vérnyomáscsökkenést okozhatnak.
Az 1. generációs hisztamin H 1 -receptorok blokkolói hatékonyak az allergiás nátha (hatékonyság kb. 80%), kötőhártya-gyulladás, viszketés, dermatitis és csalánkiütés, angioödéma, bizonyos típusú ekcéma, anafilaxiás sokk, ödéma megelőzésében és kezelésében. hipotermia okozta. Az első generációs hisztamin H 1 -receptorainak blokkolóit szimpatomimetikumokkal együtt alkalmazzák allergiás orrfolyás kezelésére. A piperazin* és a fenotiazin* származékok a hirtelen mozgások okozta hányinger, hányás és szédülés megelőzésére szolgálnak Meniere-kórban, altatás utáni hányás, sugárbetegség és reggeli hányás terhes nőknél.
Ezeknek a gyógyszereknek a helyi alkalmazása során figyelembe veszik viszketésgátló, érzéstelenítő és fájdalomcsillapító hatásukat. Nem ajánlott hosszú ideig használni őket, mivel sok közülük túlérzékenységet okozhat, és fényérzékenyítő hatású.
Az 1. generációs hisztamin H-receptor blokkolók farmakokinetikája
Az első generációs hisztamin H 1 -receptorainak blokkolói rövid hatástartamban különböznek a második generációs gyógyszerektől, és a klinikai hatás viszonylag gyorsan jelentkezik. Ezeknek a gyógyszereknek a hatása átlagosan a gyógyszer bevétele után 30 perccel jelentkezik, 1-2 órán belül éri el a csúcsot.Az első generációs antihisztaminok hatásideje 4-12 óra.metabolizmus és kiválasztódás a vesén keresztül.
A hisztamin első generációs H1-receptor blokkolóinak többsége jól felszívódik a gyomor-bél traktusból. Ezek a gyógyszerek átjutnak a BBB-n, a placentán, és bejutnak az anyatejbe is. Ezeknek a gyógyszereknek a legnagyobb koncentrációja a tüdőben, a májban, az agyban, a vesében, a lépben és az izmokban található.
A hisztamin I generáció H 1 -receptorainak legtöbb blokkolója 70-90%-ban metabolizálódik a májban. Mikroszomális enzimeket indukálnak, amelyek hosszan tartó használat esetén csökkenthetik terápiás hatásukat, valamint más gyógyszerek hatását. Számos antihisztamin metabolitja 24 órán belül kiválasztódik a vizelettel, és csak kis mennyiségben ürül változatlan formában.
Mellékhatások és ellenjavallatok a kinevezéshez
Az első generációs hisztaminreceptorok H 1-blokkolói által okozott mellékhatásokat a táblázat mutatja be. 19-4.
19-4. táblázat. Az 1. generációs antihisztaminok gyógyszermellékhatásai
 A hisztamin H1 receptor blokkolók nagy dózisai izgatottságot és görcsöket okozhatnak, különösen gyermekeknél. Ezekkel a tünetekkel a barbiturátokat nem szabad használni, mivel ez additív hatást és a légzőközpont jelentős depresszióját okozza. A ciklizin* és a klórciklizin* teratogén hatású, ezért terhes nőknél nem alkalmazható hányás esetén.
A hisztamin H1 receptor blokkolók nagy dózisai izgatottságot és görcsöket okozhatnak, különösen gyermekeknél. Ezekkel a tünetekkel a barbiturátokat nem szabad használni, mivel ez additív hatást és a légzőközpont jelentős depresszióját okozza. A ciklizin* és a klórciklizin* teratogén hatású, ezért terhes nőknél nem alkalmazható hányás esetén.
Gyógyszerkölcsönhatások
Az I. generációs hisztamin H 1 -receptorok blokkolói erősítik a kábító fájdalomcsillapítók, etanol, altatók, nyugtatók hatását. Fokozza a központi idegrendszeri stimulánsok hatását gyermekeknél. Hosszan tartó használat esetén ezek a gyógyszerek csökkentik a szteroidok, antikoagulánsok, fenilbutazon (butadion *) és más, a májban metabolizálódó gyógyszerek hatékonyságát. Antikolinerg szerekkel kombinált alkalmazásuk hatásuk túlzott fokozódásához vezethet. A MAO-gátlók fokozzák az antihisztaminok hatását. Néhány első generációs gyógyszer felerősíti az adrenalin és a noradrenalin hatását a szív- és érrendszerre. Az első generációs hisztamin H1-receptor blokkolókat az allergia klinikai tüneteinek, különösen az atópiás bronchiális asztmát gyakran kísérő rhinitis megelőzésére írják fel, az anafilaxiás sokk enyhítésére.
Antihisztaminok II és III generáció
A második generációs gyógyszerek közé tartozik a terfenadin*, az asztemizol*, a cetirizin, a mekvipazin*, a fexofenadin, a loratadin, az ebasztin, valamint a harmadik generációs hisztamin H1-receptor-blokkolók – fexofenadin (telfast*).
A hisztamin II-es és III-as generációs H 1 -receptor-blokkolók következő jellemzői különböztethetők meg:
Magas specificitás és nagy affinitás a H 1 hisztamin receptorokhoz, nincs hatással a szerotonin és m-kolinerg receptorokra;
A klinikai hatás gyors megjelenése és a hatás időtartama, amelyet általában a nagyfokú fehérjekötődéssel, a gyógyszer vagy metabolitjának szervezetben történő felhalmozódásával és késleltetett kiválasztódásával érnek el;
Minimális nyugtató hatás a gyógyszerek terápiás dózisban történő alkalmazásakor; egyes betegek mérsékelt álmosságot tapasztalhatnak, ami ritkán a gyógyszer abbahagyásának oka;
Tachyphylaxia hiánya hosszan tartó használat esetén;
Az a képesség, hogy blokkolja a káliumcsatornákat a szív vezetési rendszerének sejtjeiben, ami az intervallum megnyúlásával jár Q-Tés a szívritmus megsértése ("pirouette" típusú kamrai tachycardia).
táblázatban. A 19-5. ábrák a hisztamin II generáció néhány H1-receptor blokkolójának összehasonlító leírását mutatják be.
19-5. táblázat. A hisztamin II generációs H1-receptor blokkolók összehasonlító jellemzői
 A táblázat vége. 19-5
A táblázat vége. 19-5
 A II generációs hisztamin H-receptor blokkolók farmakodinámiája
A II generációs hisztamin H-receptor blokkolók farmakodinámiája
Az asztemizol * és a terfenadin * nem rendelkezik kolin- és β-adrenerg blokkoló hatással. Az astemizol * csak nagy dózisokban blokkolja az α-adrenerg és szerotonin receptorokat. A hisztamin II generációs H1-receptor-blokkolók gyenge terápiás hatást fejtenek ki bronchiális asztmában, mivel a hörgők és a hörgőmirigyek simaizomzatára nemcsak a hisztamin, hanem a leukotriének, a vérlemezke-aktiváló faktor, a citokinek és más mediátorok is hatással vannak. a betegség kialakulása. Csak a hisztamin H 1 -receptorainak blokkolók alkalmazása nem garantálja az allergiás hörgőgörcs teljes enyhítését.
A hisztamin II generációs H 1 -receptor blokkolók farmakokinetikájának jellemzői A hisztamin II generációs H 1 -receptorok összes blokkolója hosszú ideig (24-48 óra) hat, és a hatás kialakulásának ideje rövid - 30-60 perc. Az asztemizol* körülbelül 80%-a az utolsó adag beadása után 14 nappal, a terfenadin* pedig 12 nap múlva ürül ki. Ezeknek a gyógyszereknek a kumulatív hatása, amely a központi idegrendszer funkcióinak megváltoztatása nélkül jelentkezik, lehetővé teszi, hogy széles körben alkalmazzák őket a járóbeteg-gyakorlatban szénanáthában, csalánkiütésben, rhinitisben, neurodermatitisben stb. A II generációs hisztamin H 1 -receptorainak blokkolóit bronchiális asztmában szenvedő betegek kezelésére alkalmazzák, egyedi dózisválasztással.
A hisztamin II generációs H 1 -receptorok blokkolóira a blokkolás miatt eltérő mértékben a kardiotoxikus hatás jellemző.
a kardiomiociták minden káliumcsatornáját, és az intervallum megnyúlásával fejezzük ki Q-Tés aritmia az elektrokardiogramon.
Ennek a mellékhatásnak a kockázata nő, ha az antihisztaminok és a citokróm P-450 3A4 izoenzim inhibitorai (1.3. függelék): gombaellenes szerek (ketokonazol és itrakonazol *), makrolidok (eritromicin, oleandomicin és klaritromicin), antidepresszánsok (flux) és paroxetin), grapefruitlé fogyasztásakor, valamint súlyos májműködési zavarban szenvedő betegeknél. A fenti makrolidok asztemizollal * és terfenadinnal * kombinált alkalmazása az esetek 10% -ában kardiotoxikus hatáshoz vezet, amely az intervallum megnyúlásával jár. QT. Az azitromicin és a diritromicin * olyan makrolidok, amelyek nem gátolják a 3A4 izoenzimet, ezért nem okoznak intervallum megnyúlást Q-T a második generációs hisztamin H 1 -receptorainak blokkolóival egyidejűleg szedve.
A "" kifejezéssel kombinált gyógyszerek antihisztaminok”, meglepően gyakoriak az otthoni gyógyszeres szekrényekben. Ugyanakkor az ezeket a szereket használók túlnyomó többségének fogalma sincs sem a hatásukról, sem arról, hogy mit jelent az „antihisztaminok” szó általában, vagy arról, hogy mindez mire vezethet.
A szerző nagy örömmel írná le nagybetűkkel a szlogent: „az antihisztaminokat csak orvos írhatja fel, és szigorúan az orvos előírásai szerint használhatja”, ami után golyót tesz, és lezárja a cikk témáját. De egy ilyen helyzet nagyon hasonló lesz az Egészségügyi Minisztérium dohányzással kapcsolatos számos figyelmeztetéséhez, ezért tartózkodunk a szlogenektől, és áttérünk az orvosi ismeretek hiányosságainak pótlására.
Tehát az előfordulás
allergiás reakciók nagyrészt annak köszönhető, hogy bizonyos anyagok hatása alatt ( allergének) az emberi szervezetben bizonyos biológiailag aktív anyagok termelődnek, amelyek viszont a fejlődéshez vezetnek allergiás gyulladás. Több tucat ilyen anyag létezik, de közülük a legaktívabb hisztamin. Egészséges emberben hisztamin nagyon specifikus sejtekben (az úgynevezett hízósejtekben) inaktív állapotban van. Allergénnel érintkezve a hízósejtek hisztamint szabadítanak fel, ami allergiás tünetekhez vezet. Ezek a tünetek nagyon változatosak: duzzanat, bőrpír, kiütés, köhögés, orrfolyás, hörgőgörcs, vérnyomáscsökkenés stb.
Az orvosok meglehetősen hosszú ideje olyan gyógyszereket használnak, amelyek befolyásolhatják a hisztamin metabolizmusát. Hogyan lehet befolyásolni? Először is a hízósejtek által felszabaduló hisztamin mennyiségének csökkentése, másodszor pedig a már aktívan hatni kezdett hisztamin megkötése (semlegesítése). Ezek a gyógyszerek egyesülnek az antihisztaminok csoportjában.
Így az antihisztaminok használatának fő oka
Az allergiás tünetek megelőzése és/vagy megszüntetése. Allergia bárkire és bármire: légúti allergia (valamit rosszul szívtak be), ételallergia (valamit rosszul ettek), kontaktallergia (valami rosszal kenték be), gyógyszerallergia (azzal kezelték, ami nem illett) .
Azonnal ki kell cserélni, hogy a megelőző hatása bármely
a Az antihisztaminok nem mindig olyan hangsúlyosak, hogy egyáltalán ne legyen allergia. Innen az a teljesen logikus következtetés, hogy ha ismersz egy konkrét anyagot, ami allergiát okoz nálad vagy gyermekedben, akkor az a logika, hogy ne egyél meg egy narancsfalatot suprastinnel, hanem kerüld az allergénnel való érintkezést, azaz ne egyél narancsot. Nos, ha lehetetlen elkerülni az érintkezést, például allergiás a nyárfabolyhokra, sok a nyárfa, de nem adnak szabadságot, akkor ideje kezelni.
A "klasszikus" antihisztaminok közé tartozik a difenhidramin, diprazin, suprastin, tavegil, diazolin, fenkarol. Mindezeket a gyógyszereket évek óta használják.
A tapasztalat (pozitív és negatív egyaránt) meglehetősen nagy.
A fenti gyógyszerek mindegyikének sok szinonimája van, és nincs egyetlen ismert gyógyszeripari cég sem, amely ne gyártana legalább valami antihisztamint, természetesen saját néven. A legrelevánsabb legalább két szinonimának ismerete a patikánkban gyakran forgalmazott gyógyszerek kapcsán. A pipolfenről beszélünk, amely a diprazin és a klemasztin ikertestvére, ami megegyezik a tavegil-lel.
A fenti gyógyszerek mindegyike lenyelve is fogyasztható (tabletta, kapszula, szirup), a difenhidramin kúp formájában is kapható. Súlyos allergiás reakciók esetén, amikor gyors hatásra van szükség, intramuszkuláris és intravénás injekciókat alkalmaznak (difenhidramin, diprazin, suprastin, tavegil).
Még egyszer hangsúlyozzuk: a fenti gyógyszerek mindegyikének használatának célja egy
Az allergiás tünetek megelőzése és megszüntetése. De az antihisztaminok farmakológiai tulajdonságai nem korlátozódnak az antiallergiás hatásra. Számos gyógyszer, különösen a difenhidramin, a diprazin, a suprastin és a tavegil többé-kevésbé kifejezett nyugtató (altató, nyugtató, gátló) hatással bír. És az emberek széles tömegei aktívan használják ezt a tényt, figyelembe véve például a difenhidramint, mint csodálatos altatót. A tavegil-es suprastinből is jól alszol, de drágábbak, ezért ritkábban használják.
Az antihisztaminok nyugtató hatású jelenléte különös gondosságot igényel, különösen olyan esetekben, amikor az ezeket használó személy gyors reakciót igénylő munkát végez, például autót vezet. Ennek ellenére van kiút ebből a helyzetből, mivel a diazolinnak és a fenkarolnak nagyon csekély nyugtató hatása van. Ebből következik, hogy az allergiás rhinitisben szenvedő taxisofőr számára a suprastin ellenjavallt, és a fenkarol megfelelő lesz.
Az antihisztaminok másik hatása
Más anyagok hatásának fokozásának (potencírozásának) képessége. Az általános orvosok az antihisztaminok potencírozó hatását használják a lázcsillapító és fájdalomcsillapító gyógyszerek hatásának fokozására: mindenki ismeri a sürgősségi orvosok kedvenc keverékét - analgin + difenhidramin. Bármely központi idegrendszerre ható gyógyszer antihisztaminokkal kombinálva érezhetően aktívabbá válik, könnyen előfordulhat túladagolás egészen eszméletvesztésig, koordinációs zavarok lehetségesek (ezért sérülésveszély). Ami az alkohollal való kombinációt illeti, senki sem vállalja a lehetséges következmények előrejelzését, és bármi lehet - a mély, mély alvástól a nagyon delírium tremensig.
A difenhidramin, a diprazin, a suprastin és a tavegil nagyon nemkívánatos mellékhatásokkal rendelkezik
- "szárító" hatás a nyálkahártyákon. Ezért a gyakran előforduló szájszárazság, ami általában elviselhető. De a tüdőben lévő köpet viszkózusabbá tétele már relevánsabb és nagyon kockázatos. Legalább a fent felsorolt négy antihisztamin kiütéses alkalmazása akut légúti fertőzések (hörghurut, légcsőgyulladás, gégegyulladás) esetén jelentősen növeli a tüdőgyulladás kockázatát (a vastag nyák elveszti védő tulajdonságait, elzárja a hörgőket, megzavarja azok szellőzését - kiváló feltételek a szaporodáshoz baktériumok, tüdőgyulladás kórokozói).
Az antiallergiás hatáshoz közvetlenül nem kapcsolódó hatások nagyon sokak, és minden gyógyszer esetében eltérően fejeződnek ki. Az adagolás gyakorisága és adagja változó. Egyes gyógyszerek biztonságosak a terhesség alatt, mások nem. Az orvosnak mindezt tudnia kell, a potenciális betegnek pedig óvatosnak kell lennie. A Dimedrol hányáscsillapító hatású, a diprazint mozgási betegség megelőzésére használják, a tavegil székrekedést okoz, a suprastin zöldhályogra, gyomorfekélyre és prosztata adenomára veszélyes, a fenkarol májbetegségekre nem kívánatos. A Suprastint terhes nők használhatják, a fencarol az első három hónapban nem megengedett, a tavegil egyáltalán nem megengedett ...
Minden előnyével és hátrányával együtt
antihisztaminok a fenti gyógyszerek mindegyikének két olyan előnye van, amelyek hozzájárulnak (gyógyszerek) széles körű elterjedéséhez. Először is, valóban segítenek az allergiában, másodszor, az ára meglehetősen megfizethető.
Ez utóbbi tény különösen fontos, hiszen a farmakológiai gondolkodás nem áll meg, de költséges is. Az új modern antihisztaminok nagyrészt mentesek a klasszikus gyógyszerek mellékhatásaitól. Nem okoznak álmosságot, naponta egyszer használatosak, nem szárítják ki a nyálkahártyát, antiallergén hatásuk igen aktív. Tipikus képviselők
Asztemizol (gismanal) és klaritin (loratadin). Ez az a hely, ahol a szinonimák ismerete nagyon jelentős szerepet játszhat - legalábbis a Nashensky (Kijev) loratadin és a nem Nashensky Claritin közötti árkülönbség teljesen lehetővé teszi, hogy hat hónapig előfizessen a "My Health" magazinra.
Egyes antihisztaminoknál a profilaktikus hatás jelentősen meghaladja a terápiás hatást, vagyis elsősorban allergia megelőzésére használják. Ilyen szerek közé tartozik például a nátrium-kromoglikát (intal)
A legfontosabb gyógyszer az asztmás rohamok megelőzésére. Az asztma és a szezonális allergiák megelőzésére, például bizonyos növények virágzására, gyakran használják a ketotifent (zaditen, astafen, broniten).
A hisztamin az allergiás megnyilvánulások mellett a gyomornedv szekrécióját is fokozza. Vannak antihisztaminok, amelyek szelektíven hatnak ebben az irányban, és aktívan használják a magas savasságú gastritis, a gyomor és a nyombélfekély kezelésére.
Cimetidin (Gistak), ranitidin, famotidin. A teljesség kedvéért közlöm, mivel az antihisztaminokat csak az allergia kezelésére szolgáló eszköznek tekintik, és az, hogy a gyomorfekélyt is sikeresen kezelik, minden bizonnyal sok olvasónk számára felfedezés lesz.
A fekélyellenes antihisztaminokat azonban a betegek szinte soha nem alkalmazzák önmagukban, orvosi javaslat nélkül. De az allergia elleni küzdelemben a lakosság tömeges kísérletei a testükön
Inkább szabály, mint kivétel.
Tekintettel erre a szomorú tényre, megengedek magamnak néhány tanácsot és értékes útmutatást az önkezelés szerelmeseinek.
1. Hatásmechanizmus
antihisztaminok hasonlóak, de még mindig vannak különbségek. Gyakran előfordul, hogy az egyik gyógyszer egyáltalán nem segít, és egy másik alkalmazása gyorsan pozitív hatást fejt ki. Röviden, egy nagyon specifikus gyógyszer gyakran megfelelő egy adott egyén számára, és nem mindig világos, hogy ez miért történik. Legalább ha a gyógyszer szedése után 1-2 napon nincs hatás, akkor a gyógyszert le kell cserélni, vagy (orvos javaslatára) más módszerrel vagy más gyógyszercsoportba tartozó gyógyszerekkel kezelni.
2. A lenyelés sokfélesége:
Fenkarol
napi 3-4 alkalommal;
Difenhidramin, diprazin, diazolin, suprastin
napi 2-3 alkalommal;
2-szer egy nap;
Asztemizol, klaritin
1 naponta.
3. Átlagos egyszeri adag felnőtteknek
1 tabletta. Nem adok gyerekeknek adagot. A felnőttek bármennyit kísérletezhetnek magukon, de én nem járulok hozzá a gyerekeken végzett kísérletekhez, gyerekeknek csak orvos írhat fel antihisztaminokat. Ad egy adagot.
4. Fogadás és étkezés.
Phencarol, diazolin, diprazine
Étkezés után.
Suprastin
Evés közben.
Astemizol
Reggel éhgyomorra.
A Dimedrol, Claritin és Tavegil bevitele alapvetően nincs összefüggésben az étkezéssel.
5. Felvételi feltételek. Alapvetően bármelyik
egy antihisztamint (természetesen a profilaktikusan használtakat kivéve) nincs értelme 7 napnál tovább szedni. Egyes farmakológiai források azt jelzik, hogy 20 napig lehet nyelni, mások arról számolnak be, hogy az antihisztaminok szedésének 7. napjától kezdődően maguk is allergia forrásává válhatnak. Látszólag a következő az optimális: ha 5-6 napos szedés után nem szűnik meg az allergia elleni szerek iránti igény, akkor gyógyszert kell cserélni,
5 napig ittunk difenhidramint, áttértünk suprastinre stb - szerencsére van miből válogatni.
6. Nincs értelme használni
antihisztaminok "minden esetre" antibiotikumokkal együtt. Ha kezelőorvosa antibiotikumot ír fel, és Ön allergiás rá, azonnal hagyja abba a szedését. Az antihisztamin gyógyszer lelassítja vagy gyengíti az allergia megnyilvánulásait: később észrevesszük, hogy lesz időnk több antibiotikumot beadni, akkor hosszabb ideig kezeljük.
7. A védőoltásokra adott reakcióknak általában semmi közük az allergiához. Tehát nem szükséges profilaktikusan a tavegils-suprastineket gyermekekbe adni.
8. És az utolsó. Kérjük, tartsa távol az antihisztaminokat gyermekektől.
Az orvosi statisztikák szerint az allergiás reakciók száma folyamatosan növekszik - ez a környezeti helyzet állandó romlásával és a civilizációs körülmények között az immunitás csökkenésével jár.
A Suprastin tökéletesen enyhíti a viszketést, felgyorsítja a bőrkiütések megszabadulásának folyamatát. Ez a gyógyszer csecsemők (30 napos kortól) kezelésére engedélyezett, de az adagolást szigorúan egyéni alapon kell kiválasztani - az orvos figyelembe veszi a baba életkorát és súlyát.
A kérdéses antihisztamint a bárányhimlő elleni komplex terápia összetevőjeként használják (csillapítja a viszketést), a "troychatka" része - a testhőmérséklet csökkentésére használt anyag.
Jegyzet:A Suprastin kategorikusan ellenjavallt terhes nők és szoptatás alatt álló nők számára.
Tavegil
Ugyanolyan esetekben használják, mint a suprastint. Hosszú antihisztamin hatása van - a hatás 12 órán át fennáll. A Tavegil nem okoz vérnyomáscsökkenést, és hipnotikus hatása kevésbé kifejezett, mint a Suprastiné.
Gyermekkorban a kérdéses gyógyszert 1 éves kortól használják - a csecsemőknek szirupot írnak fel, és a 6 évesnél idősebb gyermekek tablettákat is használhatnak. Az adagot a kezelőorvos választja ki, figyelembe véve a beteg korát és súlyát.
jegyzet:A Tavegil terhesség alatt történő alkalmazása szigorúan tilos.
Fenkarol
Ettől a gyógyszertől az antihisztamin hatás hosszabb, mivel nem csak a hisztamin receptorokat blokkolja, hanem egy specifikus enzimet is beindít, amely képes a hisztamint hasznosítani. A Fenkarol nem okoz hipnotikus és nyugtató hatást, antiaritmiás szerként használható.
A figyelembe vett antiallergén gyógyszert minden típusú allergia kezelésére használják, különösen értékes a kezelésben. A Fenkarol a parkinsonizmus komplex terápiájának része, sebészetben is alkalmazzák - az érzéstelenítéshez orvosi előkészítést kapnak.
Gyermekkorban ezt a gyógyszert 12 hónapos kortól írják fel, tanácsos a csecsemőknek narancs ízű szuszpenziót adni. A gyógyszer adagját és időtartamát a kezelőorvos határozza meg.
Jegyzet:A Fenkarol kategorikusan ellenjavallt a terhesség első trimeszterében, a második és harmadik trimeszterben pedig csak szakember felügyelete mellett alkalmazható allergia kezelésére.
Fenistil
Ezt a gyógyszert a következők kezelésére használják:
- minden típusú allergia;
- (csillapítja a viszketést);
A Fenistil csak a kezelés kezdetén okoz álmosságot, szó szerint néhány nap múlva a nyugtató hatás eltűnik. A Fenistilnek számos mellékhatása van:
- a szájnyálkahártya súlyos szárazsága;
- izomgörcsök.
Ezt a gyógyszert tabletták, gyermekeknek szánt cseppek, gél és krém formájában állítják elő. A Fenistil legújabb gyógyszeres formáit rovarcsípésre használják, ill.
Gyermekek számára a Fenistil-t egy hónapos kortól cseppek formájában írják fel, ha a beteg 12 évesnél idősebb, akkor tablettákat írnak fel neki.
Jegyzet:terhesség alatt a Fenistil gél és cseppek formájában alkalmazható, a második trimesztertől csak a nő életét veszélyeztető állapotok - Quincke ödéma, akut ételallergia - esetén lehet ilyen találkozókra kerülni.
Diazolin
Alacsony antihisztamin aktivitással rendelkezik, de sok mellékhatása van:
- szédülés;
- cardiopalmus;
- gyakori vizelés.
A diazolinnak van egy bizonyos előnye is - nem okoz álmosságot, ezért felírható pilóták és vezetők allergiás reakcióinak kezelésére. A kérdéses gyógyszer antiallergiás hatásának időtartama legfeljebb 8 óra.
A Diazolin 2 éves kortól írható fel, 5 éves korig jobb, ha a gyermekeket szuszpenzió formájában adják, az idősebbeknek tablettákat is fel lehet ajánlani.
Jegyzet:A Diazolin kategorikusan ellenjavallt a terhesség első trimeszterében.
Annak ellenére, hogy az első generációs antihisztaminoknak sok hátránya van, az orvosi gyakorlatban aktívan használják őket: mindegyik gyógyszert alaposan tanulmányozták, a legtöbb esetben gyermekek számára engedélyezett.

Második generációs antihisztaminok
Nem nyugtatónak nevezik őket, kifejezett antihisztamin hatásuk van, amelynek időtartama gyakran eléri a 24 órát. Az ilyen gyógyszereket naponta egyszer kell bevenni, nem okoznak álmosságot és nem károsítják a figyelmet.
Leggyakrabban ezeket az alapokat ekcéma, csalánkiütés, Quincke-ödéma és szénanátha kezelésére használják. Gyakran második generációs antihisztaminokat használnak a kezelésben - tökéletesen enyhítik a viszketést. Ennek a gyógyszercsoportnak a megkülönböztető előnye, hogy nem okoznak függőséget. A második generációs antiallergiás szerek használatában is van egy árnyalat – idősebbeknek és szívbetegségben szenvedőknek nem ajánlottak.
Loratadin
A gyógyszer szelektíven hat a hisztamin receptorokra, ami lehetővé teszi a gyors hatás elérését. Tabletta és szirup formájában készül, "Claritin" vagy "Lomilan" néven értékesíthető. A szirup nagyon könnyen adagolható és gyermekeknek adható, a gyógyszer hatása a fogyasztást követő egy órán belül jelentkezik.
Gyermekkorban a Loratadint 2 éves kortól írják fel, az adagolást és az adagolás időtartamát csak a kezelőorvos határozza meg.
Jegyzet:a kérdéses antihisztamin nem ajánlott terhes nők számára a korai szakaszban (12 hétig). Szélsőséges esetekben a Loratadin alkalmazását szakember felügyelete mellett kell végezni.
Kestin
A gyógyszer számos kifejezett előnnyel rendelkezik:
- szelektíven blokkolja a hisztamin receptorokat;
- nem okoz álmosságot;
- a hatás a használat után egy órán belül észrevehető;
- antiallergén hatás 48 órán keresztül fennáll.
A gyermekgyógyászati gyakorlatban a Kestint 12 éves kora óta használják, de mérgező hatással lehet a májra és csökkentheti a pulzusszámot.
A Kestin terhesség alatt abszolút ellenjavallt.
Rupafin
A gyógyszert leggyakrabban kezelésre használják, lenyelés után gyorsan felszívódik, és az egyidejű táplálékfelvétel nagymértékben fokozza a Rupafin hatását.
A kérdéses gyógyszer nem alkalmazható 12 év alatti gyermekek és terhes nők kezelésére. Ha a gyógyszer alkalmazása szoptatott gyermekeknél szükséges, akkor ez csak szigorú orvosi felügyelet mellett lehetséges.
A második generációs antihisztaminok teljes mértékben megfelelnek a gyógyszerekkel szemben támasztott modern követelményeknek - rendkívül hatékonyak, hosszan tartó hatásúak, könnyen használhatók. Emlékeztetni kell arra, hogy az ilyen gyógyszereket szigorúan előírt adagban kell alkalmazni, mert túlzott mennyisége álmosságot és fokozott mellékhatásokat okoz.
Harmadik generációs antihisztaminok
Azonnal érdemes megemlíteni, hogy az antihisztaminok harmadik és negyedik generációra való felosztása megtalálható - ez nagyon feltételes, és nem hordoz mást, mint egy gyönyörű, hatékony marketing szlogent.
A harmadik generációs antihisztaminok a legmodernebbek közé tartoznak, nincs nyugtató hatásuk, nem befolyásolják a szív működését. Az ilyen alapokat aktívan használják minden típusú allergia, dermatitisz kezelésére, még gyermekeknél és szívbetegségekben szenvedőknél is.
Javasoljuk elolvasni:Allegra, Cetirizine, Xizal és Desloratadin - ezek a gyógyszerek a harmadik generációs antiallergiás gyógyszerekhez tartoznak. Mindezeket az alapokat rendkívül óvatosan kell használni a terhes nők számára - többnyire ellenjavallt. Ezenkívül szigorúan be kell tartani az előírt adagot, mivel annak túllépése fejfájást, szédülést és túl gyakori szívverést okozhat.
Az antihisztaminokat orvosnak kell felírnia, ő is kiválasztja az adagot, ajánlásokat ad a kezelés időtartamára vonatkozóan. Ha a beteg megsérti a kezelési rendet, akkor ez nemcsak a mellékhatások megjelenését, hanem az allergiás reakció növekedését is kiválthatja.
Tsygankova Yana Alexandrovna, orvosi megfigyelő, a legmagasabb minősítési kategória terapeutája
"HATÉKONY GYÓGYSZERTERÁPIA"; 5. sz.; 2014; 50-56.o.
T.G. Fedoskova
SSC Immunológiai Intézet, Oroszország FMBA, Moszkva
A gyulladás tüneteit befolyásoló és az allergiás és nem allergiás eredetű betegségek lefolyását szabályozó fő gyógyszerek közé tartoznak az antihisztaminok.
A cikk elemzi a modern antihisztaminok használatának tapasztalataival kapcsolatos vitatható pontokat, valamint néhány fő jellemzőt. Ez lehetővé teszi az optimális gyógyszer kiválasztásának differenciált megközelítését a különféle betegségek komplex terápiájában.
Kulcsszavak: antihisztaminok, allergiás betegségek, cetirizin, Cetrin
ANTIHISTAMINOK: MÍTOSZOK ÉS VALÓSÁG
T.G. Fedoskova
Állami Tudományos Központ Immunológiai Intézet, Szövetségi Orvosi és Biológiai Ügynökség, Moszkva
Az antihisztaminok a gyulladásos tüneteket befolyásoló és az allergiás és nem allergiás betegségek lefolyását szabályozó fő gyógyszerek közé tartoznak. Ebben a cikkben a jelenlegi antihisztaminok használatának tapasztalataival kapcsolatos vitatható kérdéseket, valamint azok néhány jellemzőjét elemezzük. Lehetővé teheti, hogy a különböző betegségek kombinált terápiájához megfelelő gyógyszereket alkalmazzanak.
kulcsszavak: antihisztaminok, allergiás betegségek, cetirizin, Cetrin
Az 1-es típusú antihisztaminokat (H1-AHP) vagy az 1-es típusú hisztamin receptor antagonistákat több mint 70 éve széles körben és sikeresen alkalmazzák a klinikai gyakorlatban. Használják az allergiás és pszeudoallergiás reakciók tüneti és alapterápiájának részeként, különböző eredetű akut és krónikus fertőző betegségek komplex kezelésében, premedikációként invazív és radiopaque vizsgálatok során, sebészeti beavatkozások során, vakcinázási mellékhatások megelőzésére. stb. Más szavakkal, a H 1 -AHP-t olyan állapotok esetén tanácsos használni, amelyeket specifikus és nem specifikus természetű aktív gyulladásos mediátorok felszabadulása okoz, amelyek közül a fő a hisztamin.
A hisztamin széles spektrumú biológiai aktivitással rendelkezik, amely a sejtfelszíni specifikus receptorok aktiválásán keresztül valósul meg. A hisztamin fő depója a szövetekben a hízósejtek, a vérben a bazofilek. A vérlemezkékben, a gyomornyálkahártyában, az endothel sejtekben és az agy neuronjaiban is jelen van. A hisztamin kifejezett vérnyomáscsökkentő hatással rendelkezik, és fontos biokémiai mediátor a különböző eredetű gyulladások minden klinikai tünetében. Ezért ennek a mediátornak az antagonistái továbbra is a legnépszerűbb farmakológiai szerek.
1966-ban igazolták a hisztamin receptorok heterogenitását. Jelenleg 4 típusú hisztamin receptor ismeretes - a G-fehérjékhez kapcsolódó receptorok szupercsaládjába tartozó H 1, H 2, H 3, H 4 (G-protein-coupled receptors -GPCR). A H 1 receptorok stimulálása hisztamin felszabadulásához és főként allergiás eredetű gyulladásos tünetek megjelenéséhez vezet. A H 2 receptorok aktiválása fokozza a gyomornedv elválasztását és savasságát. A H3 receptorok túlnyomórészt a központi idegrendszer (CNS) szerveiben vannak jelen. Ellátják a hisztamin-érzékeny preszinaptikus receptorok funkcióját az agyban, szabályozzák a hisztamin szintézisét a preszinaptikus idegvégződésekből. A közelmúltban a hisztamin receptorok egy új osztályát azonosították, amely túlnyomórészt monocitákon és granulocitákon expresszálódik, a H 4 -et. Ezek a receptorok a csontvelőben, a csecsemőmirigyben, a lépben, a tüdőben, a májban és a belekben találhatók. A H 1 -AHP hatásmechanizmusa a hisztamin H 1 receptorok reverzibilis kompetitív gátlásán alapul: megakadályozzák vagy minimalizálják a gyulladásos reakciókat, megakadályozva a hisztamin által kiváltott hatások kialakulását, hatékonyságukat pedig a hatás kompetitív gátlásának köszönhető. hisztamin specifikus H 1 receptor zónák lokuszain az effektor szöveti struktúrákban.
Jelenleg Oroszországban több mint 150 típusú antihisztamint tartanak nyilván. Ezek nem csak H 1 -AGP, hanem olyan gyógyszerek is, amelyek növelik a vérszérum hisztaminkötő képességét, valamint olyan gyógyszerek, amelyek gátolják a hisztamin felszabadulását a hízósejtekből. Az antihisztaminok sokfélesége miatt meglehetősen nehéz választani közülük a leghatékonyabb és legracionálisabb alkalmazásukat bizonyos klinikai esetekben. Ezzel kapcsolatban vannak vitatható pontok, és gyakran születnek mítoszok a H 1 -AHP használatáról, amelyeket a klinikai gyakorlatban széles körben alkalmaznak. A hazai szakirodalomban számos munka található ebben a témában, azonban ezeknek a gyógyszereknek a klinikai felhasználásáról (PM) nincs konszenzus.
Az antihisztaminok három generációjának mítosza
Sokan tévednek, amikor azt gondolják, hogy az antihisztaminoknak három generációja létezik. Néhány gyógyszergyártó cég harmadik generációs AGP-ként mutat be új gyógyszereket, amelyek a gyógyszerpiacon jelentek meg. Megkísérelték a modern AGP-k metabolitjait és sztereoizomerjeit a harmadik generációba sorolni. Jelenleg ezeket a gyógyszereket a második generációs antihisztaminoknak tekintik, mivel nincs jelentős különbség köztük és a korábbi, második generációs gyógyszerek között. Az antihisztaminokról szóló konszenzus szerint úgy döntöttek, hogy fenntartják a "harmadik generáció" elnevezést a jövőben szintetizált antihisztaminok jelölésére, amelyek valószínűleg számos kulcsfontosságú jellemzőjükben különböznek az ismert vegyületektől.
Sok különbség van az első és a második generációs AGP-k között. Ez elsősorban a nyugtató hatás megléte vagy hiánya. Az első generációs antihisztaminok szedése során a betegek 40-80% -a szubjektíven észleli a nyugtató hatást. Ennek hiánya az egyes betegeknél nem zárja ki e gyógyszerek objektív negatív hatását a kognitív funkciókra, amelyre a betegek nem panaszkodhatnak (autóvezetési, tanulási képesség stb.). A központi idegrendszer diszfunkciója még ezeknek a gyógyszereknek a minimális dózisának alkalmazása esetén is megfigyelhető. Az első generációs antihisztaminok hatása a központi idegrendszerre ugyanaz, mint alkohol és nyugtatók (benzodiazepinek stb.) alkalmazásakor.
A második generációs gyógyszerek gyakorlatilag nem hatolnak át a vér-agy gáton, így nem csökkentik a betegek szellemi és fizikai aktivitását. Ezenkívül az első és második generációs antihisztaminok különböznek a más típusú receptorok stimulálásával kapcsolatos mellékhatások meglétében vagy hiányában, a hatás időtartamában és a függőség kialakulásában.
Az első AGP-ket - fenbenzamint (Antergan), pirilamin-maleátot (Neo-Antergan) - már 1942-ben kezdték használni. Ezt követően új antihisztaminok jelentek meg a klinikai gyakorlatban. Egészen az 1970-es évekig Ebbe a gyógyszercsoportba tartozó vegyületek tucatjait szintetizálták.
Egyrészt nagy klinikai tapasztalat halmozódott fel az első generációs antihisztaminok alkalmazásában, másrészt ezek a gyógyszerek nem estek át a bizonyítékokon alapuló orvoslás modern követelményeinek megfelelő klinikai vizsgálatokban.
Az első és második generációs AGP összehasonlító jellemzőit a táblázat mutatja be. egy .
Asztal 1.
Az első és második generációs AGP összehasonlító jellemzői
| Tulajdonságok | Első generáció | Második generáció |
| Szedáció és hatása a megismerésre | Igen (minimális adagokban) | Nem (terápiás adagokban) |
| A H 1 receptorok szelektivitása | Nem | Igen |
| Farmakokinetikai vizsgálatok | Kevés | Sok |
| Farmakodinámiás vizsgálatok | Kevés | Sok |
| Különböző dózisú tudományos vizsgálatok | Nem | Igen |
| Újszülötteken, gyermekeken, idős betegeken végzett vizsgálatok | Nem | Igen |
| Használata terhes nőknél | FDA B kategória (difenhidramin, klórfeniramin), C kategória (hidroxizin, ketotifen) | FDA B kategória (loratadin, cetirizin, levocetirizin), C kategória (dezloratadin, azelasztin, fexofenadin, olopatadin) |
Jegyzet. FDA (US Food and Drug Administration) – Food and Drug Administration (USA). B kategória - a gyógyszer teratogén hatását nem észlelték. C kategória – vizsgálatokat nem végeztek.
1977 óta a gyógyszerpiac új H 1 -AHP-kkel egészült ki, amelyek egyértelmű előnyökkel rendelkeznek az első generációs gyógyszerekkel szemben, és megfelelnek az EAACI (European Academy of Allergology and Clinical Immunology) konszenzusos dokumentumaiban megfogalmazott korszerű AGP-k követelményeinek.
A mítosz az első generációs antihisztaminok nyugtató hatásának előnyeiről
Még az első generációs antihisztaminok néhány mellékhatása tekintetében is vannak tévhitek. Az első generációs H1-HPA nyugtató hatása azzal a tévhittel függ össze, hogy alkalmazásukat előnyben részesítik az egyidejű álmatlanságban szenvedő betegek kezelésében, és ha ez a hatás nem kívánatos, éjszakai alkalmazásával kiegyenlíthető. Ugyanakkor nem szabad megfeledkezni arról, hogy az első generációs antihisztaminok gátolják a REM-alvás fázisát, ami miatt az alvás fiziológiás folyamata megzavarodik, és az alvásban nincs teljes információfeldolgozás. Használatuk során légzési és szívritmuszavarok léphetnek fel, ami növeli az alvási apnoe kialakulásának kockázatát. Ezen túlmenően egyes esetekben ezeknek a gyógyszereknek a nagy dózisú alkalmazása hozzájárul a paradox izgalom kialakulásához, ami szintén negatívan befolyásolja az alvás minőségét. Figyelembe kell venni az antiallergiás hatás (1,5-6 óra) és a nyugtató hatás (24 óra) megőrzésének időtartamának különbségét, valamint azt, hogy a hosszan tartó szedáció kognitív károsodással jár.
A kifejezett szedatív tulajdonságok jelenléte megdönti azt a mítoszt, hogy tanácsos-e az első generációs H1-HPA alkalmazása idős betegeknél, akik ezeket a gyógyszereket használják, a szokásos önkezelés sztereotípiái, valamint a nem alkalmazó orvosok ajánlásai alapján. kellően tájékozott a gyógyszerek farmakológiai tulajdonságairól és a kinevezésük ellenjavallatairól. Az alfa-adrenerg receptorokra, muszkarinra, szerotoninra, bradikininre és más receptorokra gyakorolt hatások szelektivitásának hiánya miatt ezeknek a gyógyszereknek a kinevezésének ellenjavallata az idős betegek körében meglehetősen gyakori betegségek - glaukóma, jóindulatú prosztata hiperplázia. , bronchiális asztma, krónikus obstruktív tüdőbetegség stb.
A mítosz arról, hogy az első generációs antihisztaminoknak nincs helye a klinikai gyakorlatban
Annak ellenére, hogy az első generációs H1-AHP-k (legtöbbjük a múlt század közepén fejlesztették ki) képesek ismert mellékhatásokat okozni, a klinikai gyakorlatban ma is széles körben alkalmazzák őket. Ezért érvénytelen az a mítosz, hogy az AHD új generációjának megjelenésével nem marad hely az AHD előző generációjának. Az első generációs H 1 -AGP-nek van egy vitathatatlan előnye - az injekciós formák jelenléte, amelyek nélkülözhetetlenek a sürgősségi ellátásban, bizonyos típusú diagnosztikai vizsgálatok előtti premedikációban, sebészeti beavatkozásokban stb. Ezenkívül egyes gyógyszerek hányáscsillapító hatással rendelkeznek, csökkentik a fokozott szorongás állapotát, és hatásosak utazási betegségben. Az ebbe a csoportba tartozó számos gyógyszer további antikolinerg hatása a viszketés és a bőrkiütések jelentős csökkenésében nyilvánul meg viszkető dermatózisokkal, akut allergiás és toxikus reakciókkal az élelmiszerekre, gyógyszerekre, rovarcsípésekre és csípésekre. Ezeket a gyógyszereket azonban az indikációk, ellenjavallatok, a klinikai tünetek súlyosságának, életkorának, terápiás adagjának és mellékhatásainak szigorú figyelembevételével kell felírni. A kifejezett mellékhatások jelenléte és az első generációs H 1 -AGP tökéletlensége hozzájárult az új, második generációs antihisztaminok kifejlesztéséhez. A gyógyszerek fejlesztésének fő irányai a szelektivitás és specificitás növelése, a szedáció és a gyógyszerrel szembeni tolerancia (tachyphylaxia) megszüntetése voltak.
A második generációs modern H 1 -AGP képes szelektíven befolyásolni a H 1 receptorokat, nem blokkolja őket, de mivel antagonisták, „inaktív” állapotba helyezik őket anélkül, hogy megsértenék fiziológiai tulajdonságaikat, kifejezett antiallergiás tulajdonságokkal rendelkeznek. hatás, gyors klinikai hatás, hosszú ideig (24 óra) hat, nem okoz tachyphylaxiát. Ezek a gyógyszerek gyakorlatilag nem hatolnak át a vér-agy gáton, ezért nem okoznak nyugtató hatást, kognitív károsodást.
A modern, második generációs H 1 -AGP jelentős antiallergiás hatású - stabilizálja a hízósejtek membránját, elnyomja az eozinofilek által indukált interleukin-8 felszabadulását, a granulocita-makrofág telep-stimuláló faktort (Granulocyte Macrophage Colony-Stimulating Factor) GM-CSF) és a hámsejtekből származó szolubilis intercelluláris adhéziós molekula 1 (Soluble Intercellular Adhesion Molecule-1, sICAM-1), amely az első generációs H1-AHP-hez képest nagyobb hatékonyságot biztosít az allergiás betegségek alapterápiájában, a amelyekben az allergiás gyulladás késői fázisának mediátorai jelentős szerepet játszanak.
Ezenkívül a második generációs H1-AHP fontos jellemzője, hogy további gyulladáscsökkentő hatást fejtenek ki az eozinofilek és a neutrofil granulociták kemotaxisának gátlásával, csökkentik az adhéziós molekulák (ICAM-1) expresszióját az endothel sejteken, IgE-függő thrombocyta aktiváció és citotoxikus mediátorok felszabadítása. Sok orvos nem fordít erre kellő figyelmet, azonban a felsorolt tulajdonságok lehetővé teszik az ilyen gyógyszerek alkalmazását nemcsak allergiás, hanem fertőző eredetű gyulladások esetén is.
Az összes második generációs AHD azonos biztonságának mítosza
Az orvosok között tévhit él, miszerint minden második generációs H1-HPA hasonló a biztonságban. Azonban ebben a gyógyszercsoportban vannak különbségek az anyagcseréjük sajátosságaihoz kapcsolódóan. Ezek függhetnek a máj citokróm P 450 rendszer CYP3A4 enzimjének expressziójának változékonyságától. Az ilyen változatosság hátterében genetikai tényezők, a máj-eperendszer betegségei, számos gyógyszer (makrolid antibiotikumok, egyes gombaellenes szerek, vírusellenes szerek, antidepresszánsok stb.) egyidejű bevétele állhat, olyan termékek (grapefruit) vagy alkohol, amelyek gátló hatásúak. a CYP3A4 citokróm rendszer oxigenáz aktivitása P450.
A második generációs H1-AGP között vannak:
Rizs. egy. A második generációs H 1 -AGP metabolizmusának jellemzői
Az aktív metabolitok előnyei, amelyek bevitele nem jár többletterheléssel a májra, nyilvánvalóak: a hatás kifejlődésének gyorsasága és kiszámíthatósága, a különböző gyógyszerekkel és élelmiszerekkel való együttes alkalmazás lehetősége, amelyek metabolizálódnak a májban. a citokróm P450 részvétele.
A mítosz az egyes új AGP-k nagyobb hatékonyságáról
Nem igazolódott be az a mítosz sem, hogy az elmúlt években megjelent új H1-AGP szerek nyilvánvalóan hatékonyabbak a korábbiaknál. Külföldi szerzők munkái azt mutatják, hogy a második generációs H1-AHP, például a cetirizin, kifejezettebb antihisztamin aktivitással rendelkezik, mint a sokkal később megjelent második generációs gyógyszerek (2. ábra).
Rizs. 2. A cetirizin és a dezloratadin összehasonlító antihisztamin hatása a hisztamin 24 órán belüli beadása által okozott bőrreakcióra 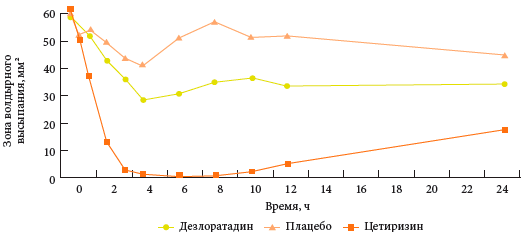
Meg kell jegyezni, hogy a második generációs H 1 -AGP között a kutatók különleges helyet tulajdonítanak a cetirizinnek. 1987-ben fejlesztették ki, és ez volt az első eredeti, erősen szelektív H 1 receptor antagonista, amely a korábban ismert első generációs antihisztamin, a hidroxizin farmakológiailag aktív metabolitján alapult. A mai napig a cetirizin az antihisztamin és antiallergén hatás egyfajta standardja, amelyet összehasonlításra használnak a legújabb antihisztamin és antiallergiás gyógyszerek kifejlesztésében. Úgy vélik, hogy a cetirizin az egyik leghatékonyabb antihisztamin H 1 gyógyszer, klinikai vizsgálatok során gyakrabban használták, a gyógyszer előnyösebb olyan betegek számára, akik rosszul reagálnak más antihisztaminokkal végzett terápiára.
A cetirizin magas antihisztamin aktivitása annak köszönhető, hogy a H 1 receptorokhoz affinitása magasabb, mint a loratadiné. Meg kell jegyezni a gyógyszer jelentős specifitását is, mivel még nagy koncentrációban sem blokkolja a szerotonint (5-HT2), a dopamint (D2), az M-kolinerg receptorokat és az alfa-1-adrenerg receptorokat. .
A cetirizin megfelel a modern második generációs antihisztaminok összes követelményének, és számos tulajdonsággal rendelkezik. Az összes ismert antihisztamin közül a cetirizin aktív metabolitja rendelkezik a legkisebb eloszlási térfogattal (0,56 l/kg), és biztosítja a H 1 receptorok teljes kihasználását és a legmagasabb antihisztamin hatást. A gyógyszert a bőrön való nagy behatolási képesség jellemzi. 24 órával az egyszeri adag bevétele után a cetirizin koncentrációja a bőrben megegyezik vagy meghaladja a vérben lévő koncentrációját. Ugyanakkor egy kúra után a terápiás hatás legfeljebb 3 napig tart. A cetirizint kifejezett antihisztamin aktivitása kedvezően különbözteti meg a modern antihisztaminok közül (3. ábra).
Rizs. 3. A második generációs H 1 -AHP egyszeri adagjának hatékonysága a hisztamin által kiváltott szaporodás visszaszorításában 24 órán keresztül egészséges férfiakban 
A mítosz az összes modern AGP magas költségéről
Bármely krónikus betegség nem alkalmas azonnali kezelésre sem. Mint ismeretes, bármely krónikus gyulladás tüneteinek elégtelen kontrollja nemcsak a beteg közérzetének romlásához vezet, hanem a gyógyszeres terápia iránti igény növekedése miatt a kezelés összköltségének növekedéséhez is. A kiválasztott gyógyszernek a leghatékonyabb terápiás hatással kell rendelkeznie, és megfizethetőnek kell lennie. Azok az orvosok, akik továbbra is elkötelezettek az első generációs H1-AHP felírása mellett, egy újabb mítoszra hivatkoznak, miszerint minden második generációs antihisztamin sokkal drágább, mint az első generációs gyógyszerek. A gyógyszerpiacon azonban az eredeti gyógyszerek mellett vannak generikumok, amelyek költsége alacsonyabb. Például jelenleg 13 generikumot tartanak nyilván a cetirizin gyógyszerből az eredeti (Zyrtec) mellett. A farmakoökonómiai elemzés eredményeit a táblázat tartalmazza. 2, a Cetrin, egy modern, második generációs AGP használatának gazdasági megvalósíthatóságáról tanúskodnak.
2. táblázat.
Az első és második generációs H1-AGP összehasonlító farmakoökonómiai jellemzőinek eredményei
| Drog | Suprastin 25 mg № 20 | Diazolin 100 mg №10 | Tavegil 1 mg № 20 | Zyrtec 10 mg 7. sz | Cetrin 10 mg № 20 |
| 1 csomag átlagos piaci értéke | 120 dörzsölje. | 50 dörzsölje. | 180 dörzsölje. | 225 dörzsölje. | 160 dörzsölje. |
| A fogadás sokfélesége | 3 r/nap | 2 r / nap | 2 r / nap | 1 r / nap | 1 r / nap |
| 1 nap terápia költsége | 18 dörzsölje. | 10 dörzsölje. | 18 dörzsölje. | 32 dörzsölje. | 8 dörzsölje. |
| 10 napos terápia költsége | 180 dörzsölje. | 100 dörzsölje. | 180 dörzsölje. | 320 dörzsölje. | 80 dörzsölje. |
Az a mítosz, hogy minden generikus gyógyszer egyformán hatékony
A generikumok felcserélhetőségének kérdése releváns az optimális modern antihisztamin gyógyszer kiválasztásakor. A farmakológiai piacon a generikumok sokfélesége miatt feltámadt az a mítosz, hogy minden generikum hozzávetőlegesen egyformán hat, így bármelyiket választhatja, elsősorban az árra koncentrálva.
Eközben a generikumok különböznek egymástól, és nem csak a farmakoökonómiai jellemzőik. A terápiás hatás stabilitását és a reprodukált gyógyszer terápiás aktivitását a technológia, a csomagolás, a hatóanyagok és a segédanyagok minősége határozza meg. A különböző gyártóktól származó gyógyszerek hatóanyagainak minősége jelentősen eltérhet. A segédanyagok összetételének bármilyen változása hozzájárulhat a biológiai hozzáférhetőség csökkenéséhez és a mellékhatások előfordulásához, beleértve a különféle természetű hiperergikus reakciókat (toxikus stb.). A generikus gyógyszernek biztonságosnak kell lennie, és egyenértékűnek kell lennie az eredeti gyógyszerrel. Két gyógyszer akkor tekinthető biológiailag egyenértékűnek, ha gyógyszerészetileg egyenértékűek, azonos biológiai hozzáférhetőséggel rendelkeznek, és azonos dózisban alkalmazva hasonlóak, megfelelő hatékonyságot és biztonságosságot biztosítva. Az Egészségügyi Világszervezet ajánlásai szerint a generikumok bioekvivalenciáját a hivatalosan bejegyzett eredeti gyógyszerhez viszonyítva kell meghatározni. A bioekvivalencia vizsgálata a terápiás ekvivalencia vizsgálatának egyik szakasza. Az FDA (Food and Drug Administration – Food and Drug Administration (USA)) évente kiadja és kiadja az "Orange Book"-t azon gyógyszerek listájával, amelyek terápiásán egyenértékűek az eredetivel. Így minden orvos optimálisan kiválaszthatja a biztonságos antihisztamin gyógyszert, figyelembe véve e gyógyszerek összes lehetséges jellemzőjét.
A cetirizin egyik rendkívül hatékony generikusa a Cetrin. A gyógyszer gyorsan, hosszú ideig hat, jó biztonsági profillal rendelkezik. A cetrin gyakorlatilag nem metabolizálódik a szervezetben, a maximális koncentrációt a szérumban egy órával a bevétel után érik el, hosszan tartó használat esetén nem halmozódik fel a szervezetben. A Cetrin 10 mg-os tablettákban kapható, felnőttek és 6 éves kor feletti gyermekek számára. A cetrin teljesen bioekvivalens az eredeti gyógyszerrel (4. ábra).
Rizs. négy. A cetirizin koncentrációjának átlagos dinamikája az összehasonlított gyógyszerek bevétele után 
A Cetrint sikeresen alkalmazzák pollenre és háztartási allergénekre érzékeny allergiás nátha, atópiás bronchiális asztmával összefüggő allergiás nátha, allergiás kötőhártya-gyulladás, csalánkiütés, beleértve a krónikus idiopátiás csalánkiütés, viszkető allergiás dermatózisok, angioödéma, valamint az alapterápia részeként. akut vírusfertőzések tüneti terápiája atópiában szenvedő betegeknél. A cetirizin generikumok teljesítménymutatóinak összehasonlítása során krónikus csalánkiütésben szenvedő betegeknél a legjobb eredményeket a Cetrin alkalmazása kapta (5. ábra).
Rizs. 5. A cetirizin készítmények klinikai hatékonyságának összehasonlító értékelése krónikus csalánkiütésben szenvedő betegeknél 
A Cetrin alkalmazásával kapcsolatos hazai és külföldi tapasztalatok azt mutatják, hogy magas terápiás hatékonysága van olyan klinikai helyzetekben, ahol a második generációs H 1 antihisztaminok alkalmazása indokolt.
Így az optimális H 1 -antihisztamin gyógyszer kiválasztásakor a gyógyszerpiacon lévő összes gyógyszer közül nem mítoszokra, hanem olyan kiválasztási kritériumokra kell alapozni, amelyek magukban foglalják a hatékonyság, a biztonság és a hozzáférhetőség közötti ésszerű egyensúly fenntartását, meggyőző bizonyítékok meglétét. alap, és kiváló minőségű gyártás. .
BIBLIOGRÁFIA:
1. Luss L.V. Az antihisztaminok kiválasztása az allergiás és pszeudoallergiás reakciók kezelésében // Russian Allergological Journal. 2009. No. 1. S. 78-84.
2. Gushchin I.S. Az antiallergiás aktivitás lehetősége és a H1-antagonisták klinikai hatékonysága // Allergológia. 2003. 1. szám C. 78-84.
3. Takeshita K., Sakai K., Bacon K.B., Gantner F. A hisztamin H4 receptor kritikus szerepe a leukotrién B4 termelésben és a hízósejt-függő neutrofil toborzásban, amelyet a zymosan in vivo indukált // J. Pharmacol. Exp. Ott. 2003. évf. 307. No. 3. P. 1072-1078.
4. Gushchin I.S. A cetirizin antiallergiás hatásának sokfélesége // Russian Allergological Journal. 2006. No. 4. S. 33.
5. Emelyanov A.V., Kochergin N.G., Goryachkina L.A. A hisztamin felfedezésének 100. évfordulójára. Az antihisztaminok klinikai használatának története és modern megközelítései // Klinikai bőrgyógyászat és venereológia. 2010. No. 4. S. 62-70.
6. Tataurshchikova N.S. Az antihisztaminok használatának modern szempontjai a háziorvosi gyakorlatban // Farmateka. 2011. No. 11. S. 46-50.
7. Fedoskova T.G. A cetirizin (Cetrin) alkalmazása az állandó allergiás rhinitisben szenvedő betegek kezelésében // Russian Allergological Journal. 2006. 5. szám C. 37-41.
8. Holgate S. T., Canonica G. W., Simons F. E. et al. Az új generációs antihisztaminok konszenzuscsoportja (CONGA): jelenlegi helyzet és ajánlások // Clin. Exp. Allergia. 2003. évf. 33. No. 9. P. 1305-1324.
9. Grundmann S.A., Stander S., Luger T.A., Beissert S. Antihisztamin kombinációs kezelés szoláris csalánkiütésre // Br. J. Dermatol. 2008. évf. 158. No. 6. P. 1384-1386.
10. Brik A., Tashkin D.P., Gong H. Jr. et al. A cetirizin, egy új hisztamin H1 antagonista hatása a légutak dinamikájára és az inhalált hisztaminra adott válaszkészségre enyhe asztmában // J. Allergy. Clin. Immunol. 1987. évf. 80. No. 1. P. 51-56.
11. Van De Venne H., Hulhoven R., Arendt C. Cetirizine in perennial atopic asthma // Eur. Ill. J. 1991. Suppl. 14. 525. o.
12. Nyílt randomizált keresztezett vizsgálat a Cetrin 0,01 tabletták (Dr. Reddy's Laboratories LTD, India) és a Zyrtec 0,01 tabletták (UCB Pharmaceutical Sector, Németország) összehasonlító farmakokinetikájára és bioekvivalenciájára, Szentpétervár, 2008.
13. Fedoskova T.G. Az akut légúti vírusfertőzések kezelésének jellemzői egész évben allergiás rhinitisben szenvedő betegeknél // Russian Allergological Journal. 2010. 5. szám P. 100-105.
14. Gyógyszerek Oroszországban, Vidal kézikönyve. M.: AstraPharmService, 2006.
15. Nekrasova E.E., Ponomareva A.V., Fedoskova T.G. A krónikus csalánkiütés racionális farmakoterápiája // Orosz Allergológiai folyóirat. 2013. No. 6. S. 69-74.
16. Fedoskova T.G. A cetirizin alkalmazása az atópiás bronchiális asztmával járó egész évben allergiás rhinitisben szenvedő betegek kezelésében // Russian Allergological Journal. 2007. No. 6. C. 32-35.
17. Elisyutina O.G., Fedenko E.S. A cetirizin atópiás dermatitiszben való alkalmazásával kapcsolatos tapasztalatok // Russian Allergological Journal. 2007. No. 5. S. 59-63.
Az antihisztaminok (hisztamin H1 receptor blokkolók) többféle besorolása létezik, bár egyik sem tekinthető általánosan elfogadottnak. Az egyik legnépszerűbb besorolás szerint az antihisztaminokat a létrehozásuk időpontja szerint I és II generációs gyógyszerekre osztják. Az első generációs gyógyszereket általában nyugtatóknak is nevezik (a domináns mellékhatás szerint), ellentétben a második generációs, nem nyugtató szerekkel.
Jelenleg az antihisztaminok harmadik generációját szokás elkülöníteni. Alapvetően új gyógyszereket tartalmaz - aktív metabolitokat, amelyeket a magas antihisztamin aktivitás mellett a nyugtató hatás hiánya és a második generációs gyógyszerekre jellemző kardiotoxikus hatás jellemez.
Az alkalmazott antihisztaminok többsége specifikus farmakológiai tulajdonságokkal rendelkezik, ami külön csoportként jellemzi őket. Ide tartoznak a következő hatások: viszketéscsillapító, dekongesztáns, görcsoldó, antikolinerg, antiszerotonin, nyugtató és helyi érzéstelenítő, valamint a hisztamin által kiváltott bronchospasmus megelőzése.
Az antihisztaminok hisztamin H1 receptor antagonisták, és ezekhez a receptorokhoz való affinitásuk sokkal kisebb, mint a hisztamin (1. táblázat). Éppen ezért ezek a gyógyszerek nem képesek kiszorítani a receptorhoz kapcsolódó hisztamint, csak a nem foglalt vagy felszabaduló receptorokat blokkolják.
1. számú táblázat. Az antihisztamin gyógyszerek összehasonlító hatékonysága a hisztamin H1 receptorok blokkolásának mértéke szempontjából
Ennek megfelelően blokkolók H 1 A hisztamin receptorok a leghatékonyabbak az azonnali allergiás reakciók megelőzésében, kialakult reakció esetén pedig megakadályozzák a hisztamin újabb adagjainak felszabadulását. Az antihisztaminok kötődése a receptorokhoz reverzibilis, és a blokkolt receptorok száma egyenesen arányos a hatóanyag koncentrációjával a receptor helyén.
A H 1 receptorok stimulálása emberben a simaizmok tónusának növekedéséhez, az érpermeabilitáshoz, a viszketés megjelenéséhez, az atrioventrikuláris vezetés lelassulásához, tachycardiához, a légutakat beidegző vagus ideg ágainak aktiválódásához, növekedéséhez vezet. a cGMP szintjében, a prosztaglandinok képződésének növekedése stb. A lapon. A lokalizációt mutató 2. sz H 1 receptorok és a rajtuk keresztül közvetített hisztamin hatásai.
2. számú táblázat. Lokalizáció H 1 receptorok és a rajtuk keresztül közvetített hisztamin hatásai
|
A H 1 receptorok lokalizációja a szervekben és szövetekben |
A hisztamin hatásai |
|
Pozitív inotróp hatás, az AV-vezetés lassulása, tachycardia, fokozott koszorúér-véráramlás |
|
|
Szedáció, tachycardia, vérnyomás-emelkedés, központi eredetű hányás |
|
|
A vazopresszin, az adrenokortikotrop hormon, a prolaktin fokozott szekréciója |
|
|
Nagy artériák |
Csökkentés |
|
kis artériák |
Pihenés |
|
Szűkület (sima izom-összehúzódás) |
|
|
Gyomor (simaizmok) |
Csökkentés |
|
Hólyag |
Csökkentés |
|
Csípőbél |
Csökkentés |
|
A hasnyálmirigy sejtjei |
A hasnyálmirigy-polipeptid fokozott szekréciója |
3. számú táblázat AGP besorolás
Első generációs antihisztaminok.
Mindegyik jól oldódik zsírokban, és a H1-hisztamin mellett a kolinerg, muszkarin és szerotonin receptorokat is blokkolja. Mivel kompetitív blokkolók, reverzibilisen kötődnek a H1 receptorokhoz, ami meglehetősen nagy dózisok alkalmazásához vezet.
Az első generáció legjellemzőbb farmakológiai tulajdonságai:
- · A nyugtató hatást az határozza meg, hogy a lipidekben könnyen oldódó első generációs antihisztaminok többsége jól áthatol a vér-agy gáton és kötődik az agy H1 receptoraihoz. Talán nyugtató hatásuk a központi szerotonin és acetilkolin receptorok blokkolása. Az első generáció nyugtató hatásának megnyilvánulási foka a különböző gyógyszereknél és a különböző betegeknél a közepestől a súlyosig változik, és alkohollal és pszichotróp szerekkel kombinálva fokozódik. Néhányukat altatóként használják (doxilamin). Ritkán szedáció helyett pszichomotoros agitáció lép fel (gyakrabban közepes terápiás dózisokban gyermekeknél és nagy toxikus dózisokban felnőtteknél). A nyugtató hatás miatt a legtöbb gyógyszert nem szabad odafigyelést igénylő feladatok során alkalmazni. Valamennyi első generációs gyógyszer fokozza a nyugtató és hipnotikus szerek, a kábító és nem kábító fájdalomcsillapítók, a monoamin-oxidáz inhibitorok és az alkohol hatását.
- A hidroxizinre jellemző szorongásoldó hatás hátterében a központi idegrendszer szubkortikális régiójának bizonyos területein az aktivitás elnyomása állhat.
- A gyógyszerek antikolinerg tulajdonságaival összefüggő atropinszerű reakciók leginkább az etanol-aminokra és az etilén-diaminokra jellemzőek. Szájszárazság és nasopharynx, vizeletvisszatartás, székrekedés, tachycardia és látásromlás nyilvánul meg. Ezek a tulajdonságok biztosítják a tárgyalt gyógymódok hatékonyságát nem allergiás nátha esetén. Ugyanakkor növelhetik az elzáródást bronchiális asztmában (a köpet viszkozitásának növekedése miatt, ami nem kívánatos a bronchiális asztmában szenvedők számára), súlyosbíthatják a glaukómát, és infravezikális elzáródáshoz vezethetnek prosztata adenomában stb.
- · A hányáscsillapító és a kilengést gátló hatás valószínűleg a gyógyszerek központi antikolinerg hatásával is összefüggésbe hozható. Egyes antihisztaminok (difenhidramin, prometazin, ciklizin, meklizin) csökkentik a vesztibuláris receptorok stimulációját és gátolják a labirintus működését, ezért utazási betegség esetén is alkalmazhatók.
- · Számos H1-hisztamin blokkoló csökkenti a parkinsonizmus tüneteit, az acetilkolin hatásának központi gátlása miatt.
- · Köhögéscsillapító hatás leginkább a difenhidraminra jellemző, amely a medulla oblongata köhögési központjára gyakorolt közvetlen hatás révén valósul meg.
- Az antiszerotonin hatás, amely elsősorban a ciproheptadinra jellemző, meghatározza annak alkalmazását migrénben.
- · A perifériás értágulattal járó alfa1-blokkoló hatás, különösen a fenotiazin antihisztaminok esetében, átmeneti vérnyomáscsökkenéshez vezethet érzékeny egyénekben.
- A helyi érzéstelenítő (kokainszerű) hatás a legtöbb antihisztaminra jellemző (a nátriumionok membránpermeabilitásának csökkenése miatt fordul elő). A difenhidramin és a prometazin erősebb helyi érzéstelenítők, mint a novokain. Mindazonáltal szisztémás kinidin-szerű hatásuk van, ami a refrakter fázis megnyúlásában és a kamrai tachycardia kialakulásában nyilvánul meg.
- · Tachyphylaxis: az antihisztamin aktivitás csökkenése hosszú távú használat esetén, ami megerősíti a 2--3 hetente váltakozó gyógyszerek szükségességét.
Meg kell jegyezni, hogy az első generációs antihisztaminok a rövid expozíciós időtartamban különböznek a második generációtól, és a klinikai hatás viszonylag gyorsan jelentkezik. Sok közülük parenterális formában kapható.
A fentiek mindegyike, az alacsony költségek, az antihisztaminok legújabb generációival kapcsolatos elégtelen köztudatosság határozza meg az első generációs antihisztaminok széles körű használatát napjainkban.
A leggyakrabban használt klórpiramin, difenhidramin, klemasztin, ciproheptadin, prometazin, fenkarol és hidroxizin.
4. számú táblázat Az 1. generáció előkészületei:
|
A gyógyszer INN |
Szinonimák |
|
Difenhidramin |
Difenhidramin, Benadryl, Allergin |
|
klemasztin |
|
|
doxilamin |
Donormil |
|
Difenilpiralin |
|
|
Brómodifenhidramin |
|
|
Dimenhidrinát |
Daedalon, Dramina, Ciel |
|
Klórpiramin |
Suprastin |
|
Antazolin |
|
|
Mepiramin |
|
|
Bromfeniramin |
|
|
Dexklór-feniramin |
|
|
Pheniramine |
Pheniramine-maleát, Avil |
|
Mebhidrolin |
Diazolin |
|
Quifenadine |
Fenkarol |
|
Szekvifenadin |
|
|
prometazin |
Prometazin-hidroklorid, Diprazin, Pipolfen |
|
Ciproheptadin |
Második generációs antihisztaminok
Az előző generációval ellentétben szinte nincs nyugtató és antikolinerg hatásuk, de különböznek a H1 receptorokra gyakorolt szelektív hatásukban. Számukra azonban különböző mértékű kardiotoxikus hatást észleltek (Ebastin (Kestin)).
Leggyakoribb tulajdonságaik a következők:
- Magas specifitás és nagy affinitás a H1 receptorokhoz, nincs hatással a kolin és szerotonin receptorokra.
- A klinikai hatás gyors megjelenése és a hatás időtartama. Megnyúlás érhető el a magas fehérjekötődés, a gyógyszer és metabolitjainak a szervezetben való felhalmozódása és a késleltetett elimináció miatt.
- Minimális szedáció a gyógyszerek terápiás dózisban történő alkalmazásakor. Ezt a vér-agy gát gyenge áthaladása magyarázza ezen alapok szerkezetének sajátosságai miatt. Egyes különösen érzékeny személyek mérsékelt álmosságot tapasztalhatnak.
- Tachyphylaxia hiánya hosszan tartó használat esetén.
- · Parenterális készítmények hiánya, de ezek egy része (azelasztin, levokabasztin, bamipin) helyileg alkalmazható.
- A kardiotoxikus hatás a szívizom káliumcsatornáinak blokkolása miatt következik be, a kardiotoxikus hatás kockázata nő, ha az antihisztaminokat gombaellenes szerekkel (ketokonazol és itrakonazol), makrolidokkal (eritromicin és klaritromicin), antidepresszánsokkal kombinálják.
Ebben az esetben az I. és II. generációs antihisztaminok alkalmazása nem kívánatos a szív- és érrendszeri betegségekben szenvedők számára. Szigorú diéta szükséges.
A második generációs antihisztaminok előnyei a következők:
- · A második generációs gyógyszerek lipofóbitásuk és a vér-agy gáton való gyenge behatolásuk miatt gyakorlatilag nincs nyugtató hatásuk, bár egyes betegeknél megfigyelhető.
- A hatás időtartama legfeljebb 24 óra, ezért a legtöbb ilyen gyógyszert naponta egyszer írják fel.
- · Függőség hiánya, amely lehetővé teszi a hosszú távú (3-12 hónapos) időpontot.
- A gyógyszer abbahagyása után a terápiás hatás egy hétig tarthat.
5. sz. táblázat. Az antihisztaminok II generációjának készítményei
III generációs antihisztaminok.
Ennek a generációnak a gyógyszerei prodrugok, azaz a szervezetben az eredeti formából gyorsan képződnek farmakológiailag aktív metabolitok, amelyek metabolikus hatást fejtenek ki.
Ha a kiindulási vegyületnek, a metabolitjaitól eltérően, nemkívánatos hatásai voltak, akkor súlyos következményekkel járhat, ha olyan körülmények lépnek fel, amelyek között koncentrációja a szervezetben megnő. Pontosan ez történt annak idején a terfenadin és az asztemizol gyógyszerekkel. Az akkor ismert H1-receptor antagonisták közül csak a cetirizin volt nem prodrug, hanem önmagában is gyógyszer. Ez az első generációs hidroxizin gyógyszer végső farmakológiailag aktív metabolitja. A cetirizin példájával kimutatták, hogy az eredeti molekula enyhe metabolikus módosítása lehetővé teszi egy minőségileg új farmakológiai gyógyszer előállítását. Hasonló megközelítést alkalmaztak egy új antihisztamin fexofenadin előállításához, amely a terfenadin végső farmakológiailag aktív metabolitján alapul. Így az alapvető különbség a III generációs antihisztaminok között az, hogy az előző generációs antihisztaminok aktív metabolitjai. Fő jellemzőjük a QT-intervallum befolyásolásának képtelensége. Jelenleg a harmadik generációs gyógyszereket a cetirizin és a fexofenadin képviseli. Ezek a gyógyszerek nem jutnak át a vér-agy gáton, ezért nem okoznak mellékhatásokat a központi idegrendszerből. Emellett a modern antihisztaminok jelentős további antiallergiás hatásokkal is rendelkeznek: csökkentik az allergén okozta hörgőgörcs súlyosságát, csökkentik a hörgők hiperreaktivitásának hatását, és nincs álmosság.
A III generációs kábítószert olyan személyek vehetik igénybe, akiknek munkája precíz mechanizmusokkal, szállítóvezetőkkel jár.
6. számú táblázat Az antihisztaminok összehasonlító jellemzői
Az allergiát a XXI. század járványának tekintik. Az antihisztaminokat széles körben használják az allergiás rohamok megelőzésére és enyhítésére.
1936-ban jelentek meg az első gyógyszerek. Az antihisztaminok több mint 70 éve ismertek, de már meglehetősen széles választékkal rendelkeznek: az I-től a III-ig generációig. Az első generációs antihisztaminok hatékonysága az allergiás betegségek kezelésében régóta bizonyított. Bár ezek a gyógyszerek mindegyike gyorsan (általában 15-30 percen belül) enyhíti az allergiás tüneteket, legtöbbjük kifejezett nyugtató hatású, és az ajánlott adagokban nem kívánt reakciókat válthat ki, valamint kölcsönhatásba léphet más gyógyszerekkel. Az első generációs antihisztaminokat elsősorban az akut allergiás reakciók enyhítésére használják.
A második generációs antihisztaminok előnyei közé tartozik a használati javallatok szélesebb köre. A gyógyszer hatása meglehetősen lassan (4-8 héten belül) alakul ki, a második generációs gyógyszerek farmakodinámiás hatásai csak túlnyomórészt in vitro igazoltak.
A közelmúltban olyan harmadik generációs antihisztaminokat hoztak létre, amelyek jelentős szelektivitással rendelkeznek, és nincsenek mellékhatásai a központi idegrendszer részéről. Az allergiás betegségek hosszú távú kezelésében indokoltabb a harmadik generációs antihisztaminok alkalmazása.
Az antihisztaminok farmakokinetikai tulajdonságai jelentősen eltérnek egymástól. A III generációs modern antihisztaminok hosszú hatástartamúak (12-48 óra).
Ezzel azonban még nincs vége, az antihisztaminok vizsgálata a mai napig tart.
allergiás betegség antihisztamin
